题目内容
19.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )| A. | 常温常压下,20 g 氖气所含有的分子数目为0.5NA | |
| B. | 常温下,46 g 乙醇含C-H键数目为6NA | |
| C. | 1.5 mol NO2与足量H2O反应,转移的电子数为NA | |
| D. | 将0.1 mol 乙酸乙酯滴加到稀硫酸中水解,生成0.1NA个CH3COOH分子 |
分析 A、氖气为单原子分子;
B、求出乙醇的物质的量,然后根据1mol乙醇中含5molC-H键来分析;
C、二氧化氮与水的反应为歧化反应;
D、乙酸乙酯在稀硫酸做催化剂的条件下的水解为可逆反应.
解答 解:A、由于氖气为单原子分子,故20 g 氖气为1 mol,故分子数为NA,故A错误;
B、46 g乙醇为1 mol,1个乙醇分子中含有5个C-H键,故C-H键数目为5NA,故B错误;
C、3NO2+H2O 2HNO3+NO,3 mol NO2转移2 mol电子,故1.5 mol NO2与足量H2O反应,转移的电子数为1 mol即NA个,故C正确;
2HNO3+NO,3 mol NO2转移2 mol电子,故1.5 mol NO2与足量H2O反应,转移的电子数为1 mol即NA个,故C正确;
D、乙酸乙酯在稀硫酸做催化剂的条件下的水解为可逆反应,不能完全水解,故生成的乙酸分子个数小于0.1NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.2015年4月,于敏获颁“影响世界华人终身成就奖”.“钚--239”是“于敏型”氢弹的重要原料.下列说法正确的是( )
| A. | 239Pu原子的原子核中含有239个质子 | |
| B. | 238Pu、239Pu和241Pu属于不同的核素 | |
| C. | 238Pu与238U在元素周期表中的位置相同 | |
| D. | 239Pu衰变成235U属于化学变化 |
7.克菌丹(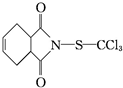 )是一种广谱性的主要用于叶面保护的杀菌剂,无药害,在果树、蔬菜及各种经济作物上使用.下列说法正确的是( )
)是一种广谱性的主要用于叶面保护的杀菌剂,无药害,在果树、蔬菜及各种经济作物上使用.下列说法正确的是( )
 )是一种广谱性的主要用于叶面保护的杀菌剂,无药害,在果树、蔬菜及各种经济作物上使用.下列说法正确的是( )
)是一种广谱性的主要用于叶面保护的杀菌剂,无药害,在果树、蔬菜及各种经济作物上使用.下列说法正确的是( )| A. | 克菌丹的分子式为C9H8O2NSCl3,属于芳香族化合物 | |
| B. | 克菌丹易溶于水,在加热条件下不能与NaOH溶液反应 | |
| C. | 克菌丹能与溴的CCl4溶液发生取代反应使之褪色 | |
| D. | 克菌丹在一定条件下能发生取代、加聚等反应 |
14.下列化学用语的表述不正确的是( )
| A. | 质子数与中子数相等的氢原子符号${:}_{1}^{1}$H | |
| B. | 乙烯的比例模型: | |
| C. | 双氧水的电子式:${H}_{•}^{•}{\stackrel{••}{\underset{••}{O}}}_{•}^{•}{\stackrel{••}{\underset{••}{O}}}_{•}^{•}$H | |
| D. | 次氯酸的结构式:H-O-Cl |
4.在MgCl2和AlCl3的混合溶液中,Cl-的物质的量为0.7mol,Al3+与Mg2+的物质的量之比为1:2.向该溶液中逐渐加入100mL 8mol•L-1 NaOH溶液,使之充分反应.下列叙述不正确是( )
| A. | 溶液中MgCl2的物质的量为0.1 mol | |
| B. | 当加入87.5 mL NaOH溶液时,沉淀质量最大 | |
| C. | 当加入90.0 mL NaOH溶液时,溶液中NaAlO2与NaCl的物质的量之比为2:35 | |
| D. | 当100 mL NaOH溶液刚好完全消耗时,Al3+恰好全部转化为Al${O}_{2}^{-}$ |
11.次磷酸盐可用于化学镀,向盛有次磷酸钠和氢氧化钠混合溶液的铁质容器中加入硫酸铜溶液,容器内壁形成牢固的铜镀层,其原理为H2PO2-+Cu2++X-→PO43-+Cu+H2O(未配平),下列有关说法正确的是( )
| A. | 该反应中次磷酸根离子得电子,表现还原性 | |
| B. | 该反应中氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 该反应每消耗3 molX,转移电子的物质的量为2mol | |
| D. | 若将硫酸铜溶液换成硝酸银溶液,容器内壁不会形成镀层 |
8.下列实验设计正确的是( )
| A. | SO2中混有CO2,通入饱和NaHSO3溶液,除CO2 | |
| B. | NaCl溶液中混有NaAlO2,通入适量CO2以将Al元素转化为Al(OH)3沉淀,过滤即可 | |
| C. | 欲制备FeCl2固体,可将过量的铁粉在少量氯气中燃烧的方式获得 | |
| D. | 除去SiO2中的Al2O3,加稍过量的稀盐酸,过滤、洗涤、干燥即可 |
9.烧杯中盛放浓度均为0.10mol/L,氯化钠和硝酸铜的混合溶液,现将该溶液以惰性电极电解,当铜离子全部在阴极下转为金属铜时,溶液的pH值为( )
| A. | 7.00 | B. | 1.00 | C. | 0.7 | D. | 1.30 |