题目内容
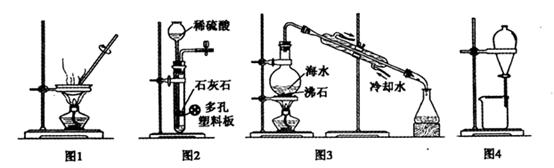
某同学设计了如图所示装置进行石油分馏的实验。

(1)指出实验装置中仪器A、B、C、D的名称:
A________、B________、C________、D________。
(2)指出该同学所设计的实验装置中存在的错误,并给予改正。
错误:①_______________________________________;
②_____________________________________________。
改正:①_______________________________________;
②_____________________________________________。
(3)实验装置改正后,进行气密性检查的方法:______________________________。
(4)蒸馏烧瓶中放入几片碎瓷片的作用是__________________________________。

(1)指出实验装置中仪器A、B、C、D的名称:
A________、B________、C________、D________。
(2)指出该同学所设计的实验装置中存在的错误,并给予改正。
错误:①_______________________________________;
②_____________________________________________。
改正:①_______________________________________;
②_____________________________________________。
(3)实验装置改正后,进行气密性检查的方法:______________________________。
(4)蒸馏烧瓶中放入几片碎瓷片的作用是__________________________________。
(1)蒸馏烧瓶 冷凝管 牛角管 锥形瓶
(2)错误:①温度计水银球伸入液面以下
②冷凝管水流方向是上口进水、下口出水
改正:①温度计水银球应与蒸馏烧瓶的支管口相平
②冷凝管水流方向应是下口进水、上口出水
(3)连接好装置后,将牛角管的下口浸入水槽中,对烧瓶的底部微热,牛角管的管口有气泡冒出,冷却后,若牛角管内形成一段水柱,说明装置的气密性良好
(4)防止暴沸
(2)错误:①温度计水银球伸入液面以下
②冷凝管水流方向是上口进水、下口出水
改正:①温度计水银球应与蒸馏烧瓶的支管口相平
②冷凝管水流方向应是下口进水、上口出水
(3)连接好装置后,将牛角管的下口浸入水槽中,对烧瓶的底部微热,牛角管的管口有气泡冒出,冷却后,若牛角管内形成一段水柱,说明装置的气密性良好
(4)防止暴沸
分馏时要特别注意:温度计的水银球要与蒸馏烧瓶的支管口相平;冷凝管的水流应是下进上出;并且要加入几片碎瓷片来防止暴沸。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

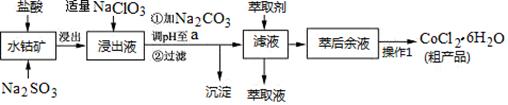


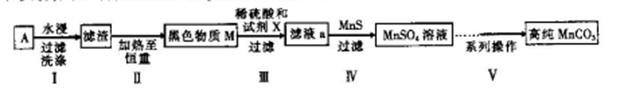

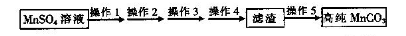
 已除干净; 操作4:___________________;
已除干净; 操作4:___________________;