��Ŀ����
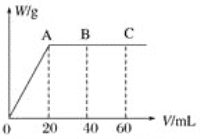
����Ŀ��Ϊ�����Ž��з�����Ԫ�����ڱ�����150���꣬���Ϲ��������2019��Ϊ�����ʻ�ѧԪ�����ڱ�������IYPT2019����Ԫ�����ڱ��������������Ϣ���ɣ��������漰��Ԫ�ؾ�Ϊ��ѧ��ѧ����������Ԫ��(����ĸx�ȱ�ʾ)ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯��ͼ��ʾ������˵������ȷ����

A.Ԫ�����ڱ���7�����ڣ�16���壬����118��Ԫ�أ��������ǽ���Ԫ��
B.x��e��ɵĻ������������ӻ�����û�������н�ǿ�Ļ�ԭ��
C.d��f��g��h�����Ӱ뾶˳��g��h��d��f
D.y��z��h������⻯��ķе�h��z��y
���𰸡�D
��������
���ڶ�����Ԫ�أ�x��e�ԣ�1�ۣ�λ��IA�壬y�ԣ�4�ۣ�λ��IVA�壬z�ԣ�5�ۣ�λ��VA�壬d��g�ԣ�2�ۣ�λ��VIA��f�ԣ�3�ۣ�λ��IIIA�壬h�ԣ�1�ۣ�λ��VIIA�壬ͬ���ڴ�������ԭ�Ӱ뾶���μ�С��ͬ������ϵ���ԭ�Ӱ뾶������ͼ����Ϣ�������ƶϳ�x��H��y��C��z��N��d��O��e��Na��f��Al��g��S��h��Cl���ݴ˷�����
���ڶ�����Ԫ�أ�x��e�ԣ�1�ۣ�λ��IA�壬y�ԣ�4�ۣ�λ��IVA�壬z�ԣ�5�ۣ�λ��VA�壬d��g�ԣ�2�ۣ�λ��VIA��f�ԣ�3�ۣ�λ��IIIA�壬h�ԣ�1�ۣ�λ��VIIA�壬ͬ���ڴ�������ԭ�Ӱ뾶���μ�С��ͬ������ϵ���ԭ�Ӱ뾶������ͼ����Ϣ�������ƶϳ�x��H��y��C��z��N��d��O��e��Na��f��Al��g��S��h��Cl��
A. Ԫ�����ڱ���7���б�ʾ7�����ڣ�18���б�ʾ16���壨IA-VIIA��IB-VIIB��VIII��8��9��10�У���0�壩��2+8+8+18+18+32+32����118��Ԫ�أ����ǽ���Ԫ�ؽ���80���֣���A˵����ȷ��
B. x��e�����NaH��NaH�����ӻ����NaH������-1�ۣ����NaH���н�ǿ�ĵĻ�ԭ�ԣ���B˵����ȷ��
C. d��f��g��h�����ӷֱ���O2-��Al3+��S2-��Cl-���ó�S2-��Cl-��O2-��Al3+����d��f��g��h�����Ӱ뾶˳��g��h��d��f����C˵����ȷ��
D. y��z��h������⻯��ֱ���CH4��NH3��HCl�����Ӿ���е�ĸ�����뷶�»����йأ�Ҫ�Ƚ����ǵķе�ߵͣ�һ���ȿ�����������������ٱȽ���Է���������NH3���Ӽ�������ܼ����������������NH3�е���ߣ����HCl����Է�������Ҫ��CH4��Է��������е�HCl����CH4�����NH3��HCl��CH4����y��z��h������⻯��ķе�z��h��y����D˵������
�𰸣�D

 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�