题目内容
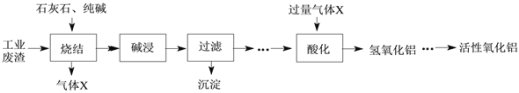
【题目】转鼓指数是反映烧结矿的机械强度的物理性能指标,其值越大,机械强度越好。某炼钢厂的工业废渣中主要含有Al2O3、Fe2O3、SiO2,对该废渣进行处理来获取活性氧化铝,其流程如下:
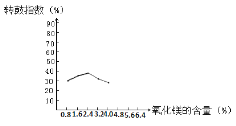
(1)烧结时往往需要加入MgO以提高烧结产物的转鼓指数,下图是转鼓指数与MgO含量的关系曲线。根据此图可知,最适宜的MgO含量是____%。
(2)烧结产物主要有NaAlO2、Ca2SiO4、NaFeO2及气体X。气体X是____。
(3)碱浸前需将烧结产物进行粉碎,其目的是____。碱浸过程中,NaFeO2可与水反应生成NaOH和一种含铁的化合物,该含铁的化合物是____。
(4)酸化时发生反应的离子方程式是____。
【答案】2.4 CO2 增大反应物接触面积,加快反应速率,提高烧结产物的浸出率 Fe(OH)3 AlO2- + CO2+ 2H2O= Al(OH)3↓+HCO3-
【解析】
(1)根据题干可知转鼓指数越大,机械强度越好,来确定最适宜的氧化镁含量。
(2)根据烧结产物主要有NaAlO2、Ca2SiO4、NaFeO2可知石灰石,纯碱与Al2O3、Fe2O3、SiO2发生反应确定气体产物。
(3)将烧结产物进行粉碎用来增大反应物的接触面积,加快反应速率并且提高烧结产物浸出率;碱浸过程中,NaFeO2与水反应生成NaOH和一种含铁的化合物,可以确定是弱酸强碱盐发生了水解。
(4)根据强酸制弱酸原理书写离子方程式,要注意通入了过量二氧化碳。
(1)转鼓指数是反映烧结矿的机械强度的物理性能指标,其值越大,机械强度越好,根据图像选择最高点,确定最适宜的氧化镁含量为2.4%;
正确答案:2.4。
(2)根据题给工艺流程和信息可知,烧结过程中Al2O3、Fe2O3、SiO2与碳酸钠、碳酸钙反应化学方程式为Al2O3+Na2CO3![]() 2NaAlO2+CO2↑,Fe2O3+Na2CO3
2NaAlO2+CO2↑,Fe2O3+Na2CO3![]() 2NaFeO2+CO2↑,SiO2+2CaCO3
2NaFeO2+CO2↑,SiO2+2CaCO3![]() Ca2SiO4+2CO2↑,因此气体X为二氧化碳;
Ca2SiO4+2CO2↑,因此气体X为二氧化碳;
正确答案:CO2。
(3)碱浸前需将烧结产物进行粉碎,其目的是增大反应物的接触面积,提高烧结产物浸出率,碱浸过程中,NaFeO2完全水解生成氢氧化铁沉淀和氢氧化钠,水解反应的离子方程式为FeO2-+2H2O=Fe(OH)3↓+OH-;
正确答案:Fe(OH)3。
(4)根据题给流程知,酸化过程为偏铝酸钠溶液中通入过量二氧化碳,生成沉淀为Al(OH)3,离子方程式AlO2- + CO2+ 2H2O= Al(OH)3↓+HCO3-;
正确答案:AlO2- + CO2+ 2H2O= Al(OH)3↓+HCO3-。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
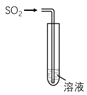
阳光试卷单元测试卷系列答案【题目】如右图所示,将SO2通入下列不同溶液中,实验现象与所得结论不正确的是
溶液 | 现象 | 结论 |
| |
A | 品红溶液 | 红色溶液褪色 | SO2有漂白性 | |
B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 | |
C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 | |
D | 滴有酚酞的NaOH溶液 | 红色溶液褪色 | SO2的水溶液呈酸性 |
A. A B. B C. C D. D
【题目】如图是铁与水蒸气反应的实验装置。在硬质玻璃管中放入还原铁粉和石棉绒(石棉绒是耐高温材料,与水、铁不反应)的混合物,加热,并通入水蒸气,就可以完成高温下铁与水蒸气反应的实验。
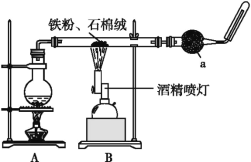
(1)已知该实验反应的反应方程式为:Fe+H2O![]() Fe3O4+H2(请配平)____。
Fe3O4+H2(请配平)____。
(2)仪器a的名称是________。
(3)某同学为了研究一定时间内铁粉的转化率,设计了如下实验:准确称量一定质量的铁粉进行反应,测量反应后生成气体的体积,计算铁粉的转化率。
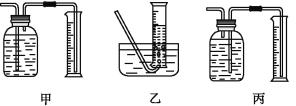
①该同学应该先点燃___(填“A”或“B”)处的酒精灯(或酒精喷灯),测量气体体积不可以选用上图中___(填“甲”“乙”或“丙”)装置。
②称取5.6 g铁粉与适量石棉绒混合,然后加热反应一段时间。若测出的气体体积在标准状况下为0.448 L,则铁粉的转化率为___。(![]() )
)
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,为探究反应后溶液中可能的阳离子,小林同学进行如下实验,请你将下表补充完整:
步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
Ⅰ.取样,滴加KSCN溶液 | 溶液不变红色 | ①Fe3O4+8H+=Fe2++2Fe3++4H2O ②____________ | Ⅲ.反应后的溶液中阳离子为_______ |
Ⅱ.取样,滴加NaOH溶液 | 刚开始无明显现象,一段时间后先出现____色沉淀,迅速变为灰绿色,最终变为______色 | ①____________ ②Fe2++2OH—=Fe(OH)2↓ ③4Fe(OH)2+2H2O+O2=4Fe(OH)3 |