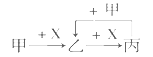题目内容
【题目】已知某烃A的产量是衡量一个国家石油化工水平的标志,能发生下列转化关系(部分反应物或生成物及反应条件已略去):
请回答下列问题:
(1)写出下列物质的结构简式:B , D;
(2)写出下列反应A→B的化学方程式 , 反应类型;
(3)写出下列反应C+E→F的化学方程式 , 反应类型 .
【答案】
(1)CH3CH2Cl;CH3CHO
(2)CH2=CH2+HCl ![]() CH3CH2Cl;加成反应
CH3CH2Cl;加成反应
(3)CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O;酯化反应
CH3COOCH2CH3+H2O;酯化反应
【解析】解:烃A的产量是衡量一个国家石油化工发展水平的标志,则A是乙烯,乙烯与HCl发生加成反应生成B为CH3CH2Cl,B发生水解反应生成C为CH3CH2OH,乙醇发生催化氧化生成D为CH3CHO,乙醛进一步发生氧化反应生成E为CH3COOH,乙酸与乙醇发生酯化反应生成F为CH3COOCH2CH3 , (1)由于上述分析可知,B的结构简式为CH3CH2Cl,D的结构简式为CH3CHO,所以答案是:CH3CH2Cl;CH3CHO;(2)乙烯与氯化氢发生加成反应生成CH3CH2Cl,方程式为CH2=CH2+HCl ![]() CH3CH2Cl,所以答案是:CH2=CH2+HCl
CH3CH2Cl,所以答案是:CH2=CH2+HCl ![]() CH3CH2Cl;加成反应;(3)在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,反应方程式为:CH3CH2OH+CH3COOH
CH3CH2Cl;加成反应;(3)在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,反应方程式为:CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O,所以答案是:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,所以答案是:CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O;酯化反应.
CH3COOCH2CH3+H2O;酯化反应.

 阅读快车系列答案
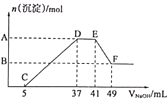
阅读快车系列答案【题目】硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质.用硼泥生产氢氧化镁的工艺流程如图所示: 
已知某些氢氧化物沉淀的pH如下表所示:
氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
Mg(OH)2 | 9.3 | 10.8 |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
(1)MgO的电子式为 .
(2)滤渣2的主要成分是 , 向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为 .
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为 .
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4 , 可以使烟气脱硫,该反应的化学方程式为 .
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为(用含有a、b的代数式表示).
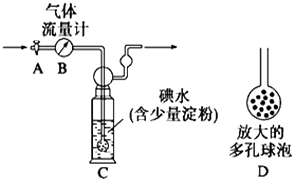
【题目】利用右图所示装置进行下列实验,能得到相应实验结论的是 ( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | Na2SO3 | KMnO4溶液褪色 | SO2有漂白性 | |
B | 浓盐酸 | KMnO4 | FeBr2溶液变为黄色 | 氧化性:Cl2 >Br2 | |
C | 稀硫酸 | 碳酸钠 | CaCl2溶液无明显变化 | CO2不与CaCl2反应 | |
D | 浓硫酸 | 蔗糖 | 溴水褪色 | 浓硫酸具有脱水性、吸水性 |
A.A
B.B
C.C
D.D