题目内容
【题目】已知:锂离子电池的总反应为:LixC+Li1-xCoO2![]() C+LiCoO2锂硫电池的总反应为:2Li+S
C+LiCoO2锂硫电池的总反应为:2Li+S![]() Li2S。有关上述两种电池说法正确的是
Li2S。有关上述两种电池说法正确的是
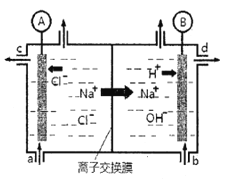
A. 锂离子电池放电时,Li+向负极迁移 B. 锂硫电池充电时,锂电极发生还原反应
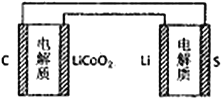
C. 理论上两种电池的比能量相同 D. 右图表示用锂离子电池给锂硫电池充电
【答案】B
【解析】A项,锂离子电池放电时,外电路中电子从负极流向正极,内电路中阴离子从正极流向负极,外电路中电流与电子方向相反,内电路中阳离子与阴离子移动方向相反,所以阳离子向正极移动,故A错误;B项,锂硫电池充电时Li2S发生反应生成S和Li,Li的化合价由+1价降到0价,所以锂电极上发生还原反应,故B正确;C项,比能量是参与电极反应的单位质量的电极材料放出电能的大小,锂硫电池放电时负极为Li,锂离子电池放电时负极为LixC,两种电池的负极材料不同,所以比能量不同,故C错误;D项,锂硫电池的正极是S,负极是Li,锂离子电池负极反应为:LixC-xe-=C+xLi+,正极反应为:Li1-xCoO2+xLi++xe-=LiCoO2,所以图中LiCoO2一端是正极,C一端是负极,所以用锂离子电池给锂硫电池充电,锂离子电池负极接原锂硫电池的负极,即C电极应连接Li电极,故D错误。

【题目】CoCl26H2O是一种饲料营养强化剂。可由水钴矿[主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等]制取,其工艺流程如下:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl26H2O熔点为86℃,加热至110﹣120℃时,失去结晶水生成CoCl2.
回答下列问题:
(1)浸出水钴矿过程中,Fe2O3发生反应的化学方程式为________________________。
(2)向浸出液中加入适量NaClO3目的是______________________________________。
(3)“加Na2CO3调pH至a”,a=______;过滤所得沉淀的主要成分为_________(填化学式)。
(4)萃取剂对金属离子的萃取与溶液pH的关系如下图所示,向“滤液”中加入该萃取剂的目的是__________,使用该萃取剂的最佳pH范围是_____(填选项字母)
A. 5.0﹣5.5 B. 4.0﹣4.5 C. 3.0﹣3.5 D. 2.0﹣2.5

(5)实验操作“操作1”为_______________、_________、过滤和减压烘干;制得的CoCl26H2O在烘干时需减压烘干的原因是________________________。