题目内容
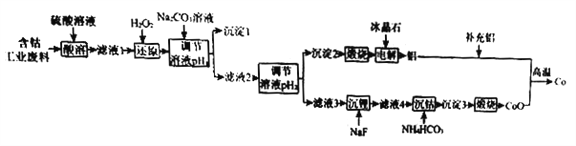
【题目】钴(Co)是重要的稀有金属,在工业和科技领域具有广泛的用途。从某含钴工业废料中回收钴的工艺流程如下:
已知:
含钴废料的成分 | |||||
成分 | Al | Li | Co2O3 | Fe2O3 | 其他不溶于强酸的杂质 |
质量分数/% | 10.5 | 0.35 | 65.6 | 9.6 | 13.95 |
Ⅱ.实验中部分离子开始沉淀和沉淀完全的pH | |||
金属离子 | Fe3+ | Co2+ | Al3+ |
开始沉淀的pH | 1.9 | 7.15 | 3.4 |
沉淀完全的pH | 3.2 | 9.15 | 4.7 |
Ⅲ.离子浓度小于等于1.0×10-5 mol·L-1时,认为该离子沉淀完全。
请回答下列问题:
(1)NaF的电子式为____________。
(2)“沉淀1”的化学式为____________________。“调节溶液pH2”的范围为_________________。
(3)“还原”时发生反应的离子方程式为_______________________。
“沉钴”时发生反应的离子方程式为________________________。
(4)制备Co时,“补充铝”的原因为_________________________。
(5)已知:l0-0.9≈0.13,则 A1(OH)3 的溶度积常数 Ksp=_____________________。
(6)Li-SOCl2电池可用于心脏起搏器,该电池的总反应可表示为::4Li+2SOCl2=4LiCl+S+SO2,其正极反应式为_____________
【答案】 ![]() Fe(OH)3 4.7≤pH≤7.15 2CO3-+H2O2=2CO2-+O2↑2H+ CO2-+2HCO3-=COCO3↓+CO2↑+H2O 原混合物中Al和Co的物质的量之比小于2:3 1.3
Fe(OH)3 4.7≤pH≤7.15 2CO3-+H2O2=2CO2-+O2↑2H+ CO2-+2HCO3-=COCO3↓+CO2↑+H2O 原混合物中Al和Co的物质的量之比小于2:3 1.3 ![]() 10-33 2SOCl2+4e-=S+SO2+4Cl-
10-33 2SOCl2+4e-=S+SO2+4Cl-
【解析】(1)NaF属于离子化合物,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)含钴工业废料用硫酸溶解后,废料中的铝、锂、氧化钴、氧化铁等被硫酸溶解,滤去残渣后有双氧水将Co3+还原为Co2+,根据部分离子开始沉淀和沉淀完全的pH,再用碳酸钠溶液调节溶液的pH,使铁离子沉淀除去,滤液2,再调节溶液的pH使铝离子沉淀,提供电解冶炼铝的原料。 “调节溶液pH2”的范围为4.7≤pH≤7.15,故答案为:Fe(OH)3;4.7≤pH≤7.15;
(3)“还原”时双氧水被Co3+氧化,反应的离子方程式为2Co3++H2O2=2Co2++O2↑+2H+,“沉钴”时碳酸氢铵与Co2+反应生成碳酸钴沉淀,反应的离子方程式为Co2++2HCO3-=CoCO3↓+CO2↑+H2O,故答案为:2Co3++H2O2=2Co2++O2↑+2H+;Co2++2HCO3-=CoCO3↓+CO2↑+H2O
(4)制备Co时的反应方程式为3CoO+2Al![]() 3Co+ Al2O3,当原混合物中Al和Co的物质的量之比小于2:3时,需要 补充铝,便于反应完全进行,故答案为:原混合物中Al和Co的物质的量之比小于2:3;
3Co+ Al2O3,当原混合物中Al和Co的物质的量之比小于2:3时,需要 补充铝,便于反应完全进行,故答案为:原混合物中Al和Co的物质的量之比小于2:3;
(5)Al3+完全沉淀时的pH=4.7,则 A1(OH)3 的溶度积常数 Ksp=1.0×10-5×(![]() )3=1.0×10-32.9=1.3
)3=1.0×10-32.9=1.3 ![]() 10-33,故答案为:1.3
10-33,故答案为:1.3 ![]() 10-33;
10-33;
(6)根据总反应4Li+2SOCl2=4LiCl+S+SO2,正极发生还原反应,SOCl2被还原生成S+SO2以及氯离子,反应式为2SOCl2+4e-=S+SO2+4Cl-,故答案为:2SOCl2+4e-=S+SO2+4Cl-。



