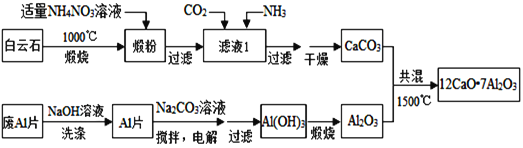
题目内容
【题目】下列实验方案正确且能达到实验目的的是( )
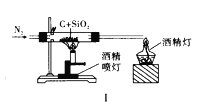
A. 图Ⅰ比较碳、硅两元素非金属性的强弱
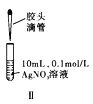
B. 图Ⅱ先滴加5滴![]() 的
的![]() 溶液,再滴加5滴
溶液,再滴加5滴![]() 的
的![]() 溶液。比较
溶液。比较![]() 与
与![]() 溶解度的大小
溶解度的大小
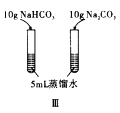
C. 图Ⅲ已知溶解度(20℃)![]() :
:![]() ;
;![]() :
:![]() 。室温下,比较
。室温下,比较![]() 和
和![]() 溶解度的大小
溶解度的大小
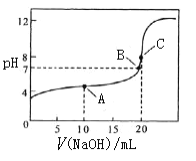
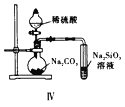
D. 图Ⅳ证明碳酸的酸性比硅酸强
【答案】D
【解析】
A、比较非金属性的强弱,要比较非金属单质的氧化性;
B、先滴加5滴![]() 的
的![]() 溶液,过滤后在沉淀中再滴加5滴
溶液,过滤后在沉淀中再滴加5滴![]() 的
的![]() 溶液,看沉淀是否转化;
溶液,看沉淀是否转化;
C、根据溶解度,可设计成加1g![]() 和
和![]() ;
;
D、二氧化碳与硅酸钠溶液反应生成硅酸。
A、碳做还原剂,硅单质做还原产物,不能比较非金属性的强弱,故A错误;
B、硝酸银是过量的,因此无法比较![]() 与
与![]() 溶解度的大小,故B错误;
溶解度的大小,故B错误;
C、![]() 的
的![]() 和
和![]() 在
在![]() 的蒸馏水中都无法完全溶解,因此无法比较溶解度的大小,根据溶解度,可设计成加1g
的蒸馏水中都无法完全溶解,因此无法比较溶解度的大小,根据溶解度,可设计成加1g![]() 和
和![]() ,故C错误;
,故C错误;
D、 碳酸和硅酸都是碳和硅最高价氧化物对应水化物,且会生成硅酸沉淀,图Ⅳ证明碳酸的酸性比硅酸强,故D正确;
故选D。

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目