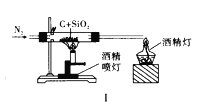
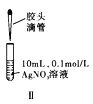
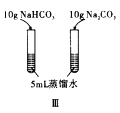
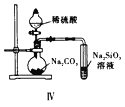
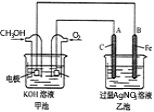
题目内容
【题目】以![]() 和
和![]() 为原料可合成尿素
为原料可合成尿素![]() ,反应为:
,反应为:![]() 。达到平衡时,
。达到平衡时,![]() 的转化率
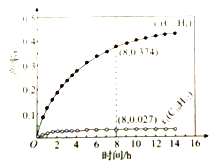
的转化率![]() 随温度变化的情况如下图。下列说法不正确的是( )
随温度变化的情况如下图。下列说法不正确的是( )

A. 该反应的![]()
B. 若y为压强,则![]()
C. 若y表示反应起始时的水碳比(![]() ,则
,则![]()
D. 在恒温恒容(2L)的容器和绝热恒容(2L)容器中,分别加入![]() 和
和![]() ,达到平衡时,恒温恒容体系中氨气的转化率大于绝热恒容体系中氨气的转化率
,达到平衡时,恒温恒容体系中氨气的转化率大于绝热恒容体系中氨气的转化率
【答案】C
【解析】
图象分析得到温度升高,氨气转化率减小说明平衡逆向进行,正反应为放热反应,压强越大平衡正向进行,氨气转化率增大,若y表示压强,则一定温度下y1大于y2,若y表示反应开始时的水碳比,升温平衡逆向进行,氨气转化率减小,一定温度下,水和二氧化碳之比越大,平衡逆向进行,氨气转化率越小,则y1小于y2。在绝热恒容体系中加入反应物,反应正向进行,产生的热量提高了体系的温度,由于是放热反应,因此不利于反应的正向进行。
A、由图像可知,氨气的转化率随温度的升高而降低,因此,该反应是放热反应,故A正确;
B、正反应方向为压强减小的变化,因此压强越大,平衡越正向移动,氨气的转化率越高,所以![]() ,故B正确;
,故B正确;
C、起始时的水碳比(![]() 越小,代表起始时
越小,代表起始时![]() 越多,则氨气的转化率越高,因此
越多,则氨气的转化率越高,因此![]() ,故C错误;
,故C错误;
D、在绝热恒容体系中加入反应物,反应正向进行,产生的热量提高了体系的温度,由于是放热反应,因此不利于反应的正向进行,氨气的转化率小于恒温恒容体系中氨气的转化率,D项正确。
故选C。

【题目】![]() 是化工合成中最重要的镍源,在实验室中模拟工业上利用金属镍废料(含镍、铁、铝)生产氯化镍晶体
是化工合成中最重要的镍源,在实验室中模拟工业上利用金属镍废料(含镍、铁、铝)生产氯化镍晶体![]() 流程如下:
流程如下:

下表列出了相关金属离子生产氢氧化物沉淀的pH:
氢氧化物 |
|
|
|
|
开始沉淀的pH | 7.6 | 2.7 | 7.1 | 3.7 |
沉淀完全的pH | 9.6 | 3.7 | 9.2 | 4.7 |
回答下列问题:
(1)加入![]() 氧化时发生反应的离子方程式为________________________,调pH的范围为____________,若调
氧化时发生反应的离子方程式为________________________,调pH的范围为____________,若调![]() ,则溶液中
,则溶液中![]() _______________。(已知
_______________。(已知![]() ,
,![]() )
)
(2)滤液A的溶质主要是______________________。
(3)操作①的实验方法依次是_____________、_____________、过滤、洗涤、干燥,操作②的实验方法是_____________。