��Ŀ����
�����ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢����ͼת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������

�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��A ��H ��
��2��д�����з�Ӧ�����ӷ���ʽ��
��Ӧ��
��Ӧ��
��3��д��D+G��H�����ӷ���ʽ�� ��
��4���ڽ���A��ˮ��Ӧ�ķ�Ӧ�У���2.3g A��ˮ��ַ�Ӧ��ת�Ƶĵ��ӵ����ʵ���Ϊ mol��

�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��A
��2��д�����з�Ӧ�����ӷ���ʽ��
��Ӧ��
��Ӧ��
��3��д��D+G��H�����ӷ���ʽ��
��4���ڽ���A��ˮ��Ӧ�ķ�Ӧ�У���2.3g A��ˮ��ַ�Ӧ��ת�Ƶĵ��ӵ����ʵ���Ϊ
���㣺������ƶ�
ר�⣺
����������A��ɫ��ӦΪ��ɫ����AΪ����Na����ˮ��Ӧ����NaOH����������DΪNaOH�������ΪH2���������������B��Ӧ�����������ʽ���BΪAl������ɫ������ΪCl2����������Ӧ���ɱ�ΪHCl��HCl����ˮ������EΪ���ᣮ��������������G��Ӧ���ɺ��ɫ����H��Fe��OH��3��������G�к���Fe3+����ת����ϵHCl��C��Ӧ����F��F��������Ӧ��������G����֪����CΪFe������FΪFeCl2������GΪFeCl3��������ʵ����ʽ����⣮
���
�⣺����A��ɫ��ӦΪ��ɫ����AΪ����Na����ˮ��Ӧ����NaOH����������DΪNaOH�������ΪH2���������������B��Ӧ�����������ʽ���BΪAl������ɫ������ΪCl2����������Ӧ���ɱ�ΪHCl��HCl����ˮ������EΪ���ᣮ��������������G��Ӧ���ɺ��ɫ����H��Fe��OH��3��������G�к���Fe3+����ת����ϵHCl��C��Ӧ����F��F��������Ӧ��������G����֪����CΪFe������FΪFeCl2������GΪFeCl3��
��1�������Ϸ�����֪AΪNa��HΪFe��OH��3���ʴ�Ϊ��Na��Fe��OH��3��
��2����Ӧ��Ϊ��������ķ�Ӧ����Ӧ�����ӷ���ʽΪFe+2H+=Fe2++H2������Ӧ��Ϊ��������������Һ�ķ�Ӧ����Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O�T2AlO2-+3H2����
�ʴ�Ϊ��Fe+2H+=Fe2++H2����2Al+2OH-+2H2O�T2AlO2-+3H2����
��3��D+G��H�ķ�Ӧ����ʽΪFeCl3+3NaOH=Fe��OH��3��+3NaCl�������ӷ���ʽΪFe3++3OH-=Fe��OH��3�����ʴ�Ϊ��Fe3++3OH-=Fe��OH��3����
��4��Na��ˮ��Ӧ�ķ���ʽΪ2Na+2H2O=2NaOH+H2������Ӧ��NaԪ�ػ��ϼ���0�����ߵ�+1�ۣ�2.3g Na��ˮ��ַ�Ӧ����0.1molNa��Ӧ����ʧȥ����Ϊ0.1mol��
�ʴ�Ϊ��0.1��
��1�������Ϸ�����֪AΪNa��HΪFe��OH��3���ʴ�Ϊ��Na��Fe��OH��3��
��2����Ӧ��Ϊ��������ķ�Ӧ����Ӧ�����ӷ���ʽΪFe+2H+=Fe2++H2������Ӧ��Ϊ��������������Һ�ķ�Ӧ����Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O�T2AlO2-+3H2����
�ʴ�Ϊ��Fe+2H+=Fe2++H2����2Al+2OH-+2H2O�T2AlO2-+3H2����
��3��D+G��H�ķ�Ӧ����ʽΪFeCl3+3NaOH=Fe��OH��3��+3NaCl�������ӷ���ʽΪFe3++3OH-=Fe��OH��3�����ʴ�Ϊ��Fe3++3OH-=Fe��OH��3����
��4��Na��ˮ��Ӧ�ķ���ʽΪ2Na+2H2O=2NaOH+H2������Ӧ��NaԪ�ػ��ϼ���0�����ߵ�+1�ۣ�2.3g Na��ˮ��ַ�Ӧ����0.1molNa��Ӧ����ʧȥ����Ϊ0.1mol��
�ʴ�Ϊ��0.1��
����������������ͼ�����ʽ����Na��Al��Fe��Cl��Ԫ�ص��ʼ��仯����֮����ת����ϵ���ԡ���ɫ��Ӧ������ɫ���塢���ɫ������Ϊͻ�ƿڲ��������ϵķ��������ƶϣ��Ѷ��еȣ�ע�����֪ʶ�����գ�

��ϰ��ϵ�д�
�����Ŀ
��ѧ��ѧ��Ҫ������ѧר�������������������йػ�ѧ�����ʹ����ȷ���ǣ�������
A��NH4Cl�ĵ���ʽ��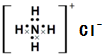 | ||
B��S2-�Ľṹʾ��ͼ�� | ||
| C��CO2�Ľṹʽ��O=C=O | ||
D��������Ϊ37����ԭ��
|
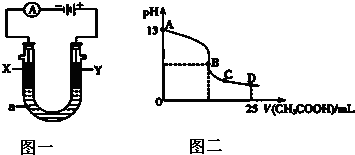
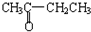
 ��
��
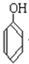 ��
��
 ��
��
 ��
��
 ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ��
ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ��