题目内容
化学科学需要借助化学专用术语来描述,下列有关化学用语的使用正确的是( )
A、NH4Cl的电子式: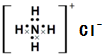 | ||
B、S2-的结构示意图: | ||
| C、CO2的结构式:O=C=O | ||
D、质量数为37的氯原子
|
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氯化铵的电子式中,氯离子最外层的8个电子没有标出;
B.硫离子的核外电子总数18,最外层为8个电子.
C.二氧化碳分子中存在两个碳氧双键,为直线型结构;
D.元素符号的左上角表示的是质量数,应该为37,左下角为质子数.
B.硫离子的核外电子总数18,最外层为8个电子.
C.二氧化碳分子中存在两个碳氧双键,为直线型结构;
D.元素符号的左上角表示的是质量数,应该为37,左下角为质子数.
解答:
解:A.氯化铵为离子化合物,电子式中需要标出离子所带电荷,阴离子需要标出最外层电子,氯化铵正确的电子式为: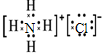 ,故A错误;
,故A错误;
B.硫离子的核电荷数为16,核外电子总数为18,最外层为8个电子,硫离子正确的结构示意图为: ,故B错误;
,故B错误;
C.二氧化碳的电子式为: ,将所有的共用电子对换成短线,即为二氧化碳的结构式,二氧化碳的结构式为:O=C=O,故C正确;
,将所有的共用电子对换成短线,即为二氧化碳的结构式,二氧化碳的结构式为:O=C=O,故C正确;
D.氯元素的核电荷数为17,质量数为37的氯原子可以表示为:1737Cl,故D错误;
故选C.
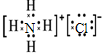 ,故A错误;
,故A错误;B.硫离子的核电荷数为16,核外电子总数为18,最外层为8个电子,硫离子正确的结构示意图为:
 ,故B错误;
,故B错误;C.二氧化碳的电子式为:
 ,将所有的共用电子对换成短线,即为二氧化碳的结构式,二氧化碳的结构式为:O=C=O,故C正确;
,将所有的共用电子对换成短线,即为二氧化碳的结构式,二氧化碳的结构式为:O=C=O,故C正确;D.氯元素的核电荷数为17,质量数为37的氯原子可以表示为:1737Cl,故D错误;
故选C.
点评:本题考查了电子式、离子结构示意图、元素符号、结构式等化学用语的判断,题目难度中等,注意掌握常见的化学用语的概念及正确的表示方法,明确离子结构示意图与原子结构示意图的区别.

练习册系列答案
相关题目
下列不能形成配位键的组合是( )
| A、Ag+、NH3 |
| B、BF3、NH3 |
| C、Co3+、CO |
| D、NH4+、H+ |
已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”.根据等电子原理,下列各组粒子结构不相似的是( )
| A、BCl3和PH3 |
| B、NH4+和CH4 |
| C、NO3-和CO32- |
| D、CO2和N2O |
分子式为C10H20O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下 能转化成C.则有机物A的可能结构有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
Al、Fe、Cu都是重要的金属元素,下列说法正确的是( )
| A、三者对应的氧化物均为碱性氧化物 |
| B、三者的单质放置在空气中均只生成氧化物 |
| C、Fe2O3与Fe3O4互为同素异形体 |
| D、常温下三者加入浓硫酸中均无明显现象 |
在密闭容器中进行反应:X2(g)+3Y2(g)?2Z(g),其中X2、Y2、Z的起始浓度分别为0.1mol?L-1、0.3mol?L-1、0.2mol?L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、c(Z)=0.5 mol?L-1 |
| B、c(Y2)=0.5 mol?L-1 |
| C、c(X2)=0.2 mol?L-1 |
| D、c(Y2)=0.6 mol?L-1 |
不能用排水集气法收集的气体是( )
| A、H2 |
| B、NO |
| C、02 |
| D、HCl |
