题目内容
下列离子方程式中正确的是( )
| A、盐酸与碳酸钡反应:CO32-+2H+=CO2↑+H2O |
| B、碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag |
| D、钠投入水中:2Na+2H2O=2Na++2OH-+H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.难溶物写化学式;
B.弱电解质写化学式;
C.电荷不守恒;
D.二者反应生成氢氧化钠和氢气.
B.弱电解质写化学式;
C.电荷不守恒;
D.二者反应生成氢氧化钠和氢气.
解答:
解:A.难溶物写化学式,离子方程式为CaCO3+2H+=CO2↑+H2O+Ca2+,故A错误;
B.弱电解质写化学式,离子方程式为CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.电荷不守恒,离子方程式为:2Ag++Cu=Cu2++2Ag,故C错误;
D.二者反应生成氢氧化钠和氢气,离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故D正确;
故选D.
B.弱电解质写化学式,离子方程式为CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.电荷不守恒,离子方程式为:2Ag++Cu=Cu2++2Ag,故C错误;
D.二者反应生成氢氧化钠和氢气,离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故D正确;
故选D.
点评:本题考查了离子方程式正误判断,明确离子方程式书写规则是解本题关键,单质、氧化物、弱电解质、气体、沉淀、络合物等都要写化学式,为易错点.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
下列物质中,属于酚类的是( )
A、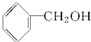 |
B、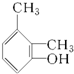 |
C、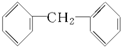 |
D、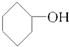 |
 为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置.下列判断合理的是( )
为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置.下列判断合理的是( )| A、左边铜片上有气泡冒出 |
| B、右边锌片上的反应为2Cl--2e-=Cl2↑ |
| C、最先观察到红色的区城是② |
| D、左右两边Cu片质量均不发生变化 |
下列各组离子中,在指定溶液中一定能大量存在的是( )
| A、澄清透明的无色溶液:ClO-、MnO4-、Al3+、SO42- |
| B、含有大量Fe3+的溶液:H+、I-、K+、Cl- |
| C、能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- |
| D、由水电离产生的c(H+)=1×10-12mol/L的溶液:NH4+、Na+、Cl-、HCO3- |
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1.0L 1.0mol?L-1 CH3COOH溶液中,CH3COOH分子数为NA |
| B、1mol Na2O2与足量H2O反应转移的电子数NA |
| C、常温常压下,22.4L氧气含有氧原子为2NA |
| D、1.8g重水(D2O)中,含有的质子数为0.1NA |
实验室保存下列药品的方法,正确的是( )
| A、氢氟酸贮存在细口玻璃瓶里 |
| B、盛溴的试剂瓶里加一些水来防止溴挥发 |
| C、盛放浓硫酸的广口瓶应当用磨口玻璃塞,不能用橡皮塞 |
| D、氯水保存在无色玻璃瓶中;液氯存贮存在钢瓶里 |
刚玉(主要成分是Al2O3)是人造红宝石和蓝宝石的原料.现用废铝屑、废酸液和废碱液来生产刚玉.为达到最大生产效率,安排生产时,废铝屑分别与废酸液作用和废碱液作用的质量比为( )
| A、1:1 | B、1:2 |
| C、1:3 | D、3:1 |
若某电能与化学能的转化装置(电解池或原电池)中发生的总反应的离子方程式是Cu+2H+═Cu2++H2↑,则下列关于该装置的有关说法中正确的是( )
| A、该装置可能是原电池,可用Cu、C作电极,电解质溶液是盐酸 |
| B、该装置可能是原电池,电解质溶液为硝酸 |
| C、该装置只能是电解池,金属铜为该电解池的阳极,K2SO4为电解质溶液 |
| D、该装置只能是电解池,金属铜为该电解池的阳极,稀H2SO4为电解质溶液 |