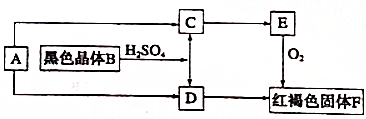
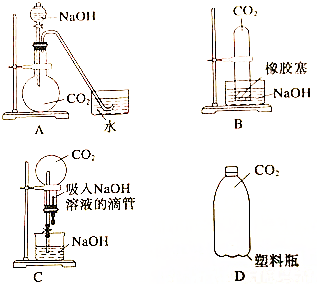
题目内容
5.学生利用如图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体.(图中夹持及尾气处理装置均已略去)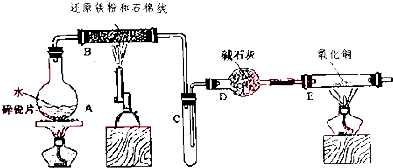
(1)回答下列问题:所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为B(填序号)
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸 D.FeCl3溶液
此步涉及反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)反应发生后装置B中发生反应的化学方程式是3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.D装置的作用:除去H2中的水蒸气.
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3•6H2O
晶体,设计流程如下:
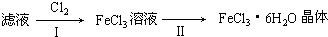
①用离子方程式表示步骤I中通入Cl2的作用Cl2+2Fe2+═2Fe3++2Cl-.
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明.向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液.你认为此方案是否合理不合理(填“合理”或“不合理”).
分析 (1)根据金属混合物中铁粉、铝粉性质的差异性进行分析、考虑,从而得出正确的结论;
(2)Fe与水蒸气反应生成Fe3O4和H2;碱石灰能干燥气体;
(3)①氯气能将二价铁离子氧化为三价铁离子;
②原溶液可能含有三价铁离子.
解答 解:(1)铁粉和铝粉都是金属,都具有金属的通性,都能和酸反应和弱碱不反应;但铝粉和铁粉的不同化学性质是:铝粉能和强碱反应生成盐和氢气,而铁粉和强碱不反应;反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:B;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)Fe与水蒸气反应生成Fe3O4和H2,反应的化学方程式是3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;碱石灰能干燥气体,除去H2中的水蒸气,
故答案为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;除去H2中的水蒸气;
(3)①氯气能将二价铁离子氧化为三价铁离子,反应的离子方程式为Cl2+2Fe2+═2Fe3++2 Cl-,
故答案为:Cl2+2Fe2+═2Fe3++2 Cl-;
②原溶液可能含有三价铁离子,使KSCN溶液液呈现红色,故不合理,
故答案为:不合理.
点评 本题考查铁及其化合物的性质实验,难度不大,注意二价Fe离子和三价Fe离子的检验.

练习册系列答案
相关题目
6.室温下,在pH=13的某溶液中,由水电离出的c(OH-)为( )
①1.0×10-7mol/L②1.0×10-6mol/L③1.0×10-1mol/L④1.0×10-13mol/L.
①1.0×10-7mol/L②1.0×10-6mol/L③1.0×10-1mol/L④1.0×10-13mol/L.
| A. | ③ | B. | ③或④ | C. | ①或③ | D. | ④ |
10.下列叙述正确的是( )
| A. | 由甲烷分子呈正四面体形结构可推知一氯甲烷分子也呈正四面体形结构 | |
| B. | 在甲烷的四种氯的取代物中,只有四氯甲烷是非极性分子 | |
| C. | 由甲烷(CH4)的氯代物有4种,可推知乙烷(结构式为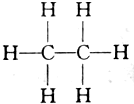 )的氯代物有6种 )的氯代物有6种 | |
| D. | 由于CH4是易燃易爆的气体,所以点燃CH4前一定要检验其纯度 |
10. 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:
熔融氧化3MnO2+KClO3+6KOH$\stackrel{高温}{→}$3K2MnO4+KCl+3H2O
加酸歧化3K2MnO4+2CO2→2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
完成下列填空:
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填序号)
a.表面皿 b.蒸发皿 c.铁坩埚 d.泥三角
(2)加酸时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O$\stackrel{通电}{→}$2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,原子利用率高.
(4)草酸钠滴定法测定高锰酸钾的质量分数步骤如下:
(已知 涉及到的反应:Na2C2O4+H2SO4→H2C2O4(草酸)+Na2SO45H2C2O4+2MnO4-+6H+→2Mn2++10CO2↑+8H2O Na2C2O4的式量:134、KMnO4的式量:158)
Ⅰ称取0.80g 的高锰酸钾产品,配成50mL溶液.
Ⅱ称取0.2014gNa2C2O4,置于锥形瓶中,加入蒸馏水使其溶解,再加入少量硫酸酸化.
Ⅲ将瓶中溶液加热到75~80℃,趁热用Ⅰ中配制的高锰酸钾溶液滴定至终点.消耗高锰酸钾溶液8.48mL,则样品中高锰酸钾的质量分数为0.700(保留3位小数).达到滴定终点的标志是无色变为紫色且半分钟不褪色.
(5)加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度偏高.(填“偏高”、“偏低”或“无影响”)
(6)将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应溶液中Mn2+的浓度随反应时间t的变化如图,其原因可能为Mn2+可能是该反应的催化剂,随着Mn2+的产生,反应速率大大加快.
 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:熔融氧化3MnO2+KClO3+6KOH$\stackrel{高温}{→}$3K2MnO4+KCl+3H2O
加酸歧化3K2MnO4+2CO2→2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
| 物质 | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度g/100g | 111 | 33.7 | 11.1 | 6.34 |
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填序号)
a.表面皿 b.蒸发皿 c.铁坩埚 d.泥三角
(2)加酸时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O$\stackrel{通电}{→}$2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,原子利用率高.
(4)草酸钠滴定法测定高锰酸钾的质量分数步骤如下:
(已知 涉及到的反应:Na2C2O4+H2SO4→H2C2O4(草酸)+Na2SO45H2C2O4+2MnO4-+6H+→2Mn2++10CO2↑+8H2O Na2C2O4的式量:134、KMnO4的式量:158)
Ⅰ称取0.80g 的高锰酸钾产品,配成50mL溶液.
Ⅱ称取0.2014gNa2C2O4,置于锥形瓶中,加入蒸馏水使其溶解,再加入少量硫酸酸化.
Ⅲ将瓶中溶液加热到75~80℃,趁热用Ⅰ中配制的高锰酸钾溶液滴定至终点.消耗高锰酸钾溶液8.48mL,则样品中高锰酸钾的质量分数为0.700(保留3位小数).达到滴定终点的标志是无色变为紫色且半分钟不褪色.
(5)加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度偏高.(填“偏高”、“偏低”或“无影响”)
(6)将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应溶液中Mn2+的浓度随反应时间t的变化如图,其原因可能为Mn2+可能是该反应的催化剂,随着Mn2+的产生,反应速率大大加快.
17.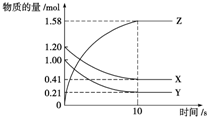 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A. | 反应在0~10 s内,用Z表示的反应速率为0.158 mol•L-1•s-1 | |
| B. | 反应在0~10 s内,X的物质的量浓度减少了0.79 mol•L-1 | |
| C. | 反应进行到10 s时,Y的转化率为79.0% | |
| D. | 反应的化学方程式为X(g)+Y(g)═Z(g) |
15.25℃时,下列各溶液中关系的叙述中,正确的是( )
| A. | 0.1 mol/L HA(某酸)溶液pH≠1,0.1 mol/L BOH(某碱)溶液中c(OH-)=0.1 mol/L,则BA(盐)溶液pH<7 | |
| B. | pH=2的盐酸与pH=l的硫酸溶液中c(H+)之比为2:1 | |
| C. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则c (Na+)+c(H+)=c(OH-)+c(CH3COO-) | |
| D. | 4种pH相同的溶液①CH3COONa ②NaHCO3 ③NaOH中c(Na+)的大小顺序是②>①>③ |