题目内容
18.下列各组元素中,原子半径依次增大的是( )| A. | Al、Si、P | B. | I、Br、Cl | C. | Na、Mg、Al | D. | O、S、Na |
分析 同周期自左而右原子半径减小,同主族自上而下原子半径增大.
解答 解:A.Al、Si、P同周期,核电荷数依次增大,原子半径依次减小,故A不符合;
B.I、Br、Cl同主族,电子层依次减小,原子半径依次减小,故B不符合;
C.Na、Mg、Al同周期,核电荷数依次增大,原子半径依次减小,故C不符合;
D.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径O<S<Na,故D符合,
故选:D.
点评 本题考查原子半径比较,比较基础,注意从结构上理解同主族、同周期元素原子半径的变化规律.

练习册系列答案
相关题目
9.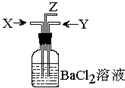 碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
 碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | |
| B. | 在Z导管出来的气体中无二氧化碳 | |
| C. | 洗气瓶中产生的沉淀是硫酸钡 | |
| D. | 洗气瓶中产生的沉淀是碳酸钡和亚硫酸钡 |
6.X、Y、Z、W四种金属片在稀盐酸中,用导线连接,可以组成原电池,实验结果如图所示:则四种金属的活泼性由强到弱的顺序为( )
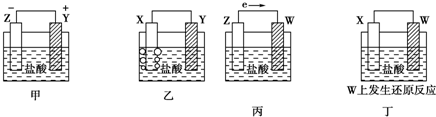

| A. | Z>Y>X>W | B. | Z>X>Y>W | C. | Z>Y>W>X | D. | Y>Z>X>W |
13.下列对于硝酸的认识,不正确的是( )
| A. | 浓硝酸和稀硝酸都具有氧化性 | |
| B. | 铜与浓硝酸的反应是置换反应 | |
| C. | 常温下,可用铁或铝制容器盛放浓HNO3 | |
| D. | 往少量的浓硝酸中加入足量的铜,生成的气体只有NO2 |
3.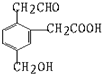 某有机物的结构式为它在一定条件下(如图)能发生的反应有( )
某有机物的结构式为它在一定条件下(如图)能发生的反应有( )
①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去.
 某有机物的结构式为它在一定条件下(如图)能发生的反应有( )
某有机物的结构式为它在一定条件下(如图)能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤ | D. | ②③④⑤ |
7.“浓硫酸可用铁制容器盛装,但久置后其外表常有严重的腐蚀现象”这句话体现了浓硫酸的( )
| A. | 强氧化性和脱水性 | B. | 强氧化性和吸水性 | ||
| C. | 难挥发性和酸性 | D. | 脱水性和吸水性 |
 和
和
 和
和

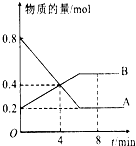 某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据
某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据