题目内容
卤族元素是典型的非金属元素,包括F、Cl、Br、I等。请回答下面有关问题
(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是_____。
(2)Br原子的M层核外电子排布式为_________。
(3)用价层电子对互斥理论判断BeCl2的构型为________,BF3分子中B-F键的键角为________。
(4)CCl4分子中碳原子的杂化方式为______,NF3分子的空间构型为_______。
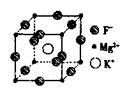
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为________。
(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是_____。
(2)Br原子的M层核外电子排布式为_________。
(3)用价层电子对互斥理论判断BeCl2的构型为________,BF3分子中B-F键的键角为________。
(4)CCl4分子中碳原子的杂化方式为______,NF3分子的空间构型为_______。
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为________。

(1)I Br Cl F
(2)3s23p63d10
(3)直线型 120。
(4)sp3 三角锥形
(5)20%
(2)3s23p63d10
(3)直线型 120。
(4)sp3 三角锥形
(5)20%
(1)非金属性越强,电负性越大,即电负由小到大的顺序是I Br Cl F;
(2)Br是第四周期元素,其M层电子排布式为3s23p63d10
(3)BeCl2中含有的孤对电子对数是(2-2×1)/2=0,所以BeCl2是直线型。BF3是平面正三角型,键角是120。
(4)CCl4是正四面体,C原子采取的是sp3杂化;N原子含有孤对电子对数是=(5-3×1)/2=1,且AB3型,所以NF3是三角锥型。
(5)该晶胞中含Mg(8×1/8)=1个,K原子个数为1,F原子数为12×1/4=3,所以其化学式为KMgF3,由化学式可算出Mg的质量分数为20%
(2)Br是第四周期元素,其M层电子排布式为3s23p63d10
(3)BeCl2中含有的孤对电子对数是(2-2×1)/2=0,所以BeCl2是直线型。BF3是平面正三角型,键角是120。
(4)CCl4是正四面体,C原子采取的是sp3杂化;N原子含有孤对电子对数是=(5-3×1)/2=1,且AB3型,所以NF3是三角锥型。
(5)该晶胞中含Mg(8×1/8)=1个,K原子个数为1,F原子数为12×1/4=3,所以其化学式为KMgF3,由化学式可算出Mg的质量分数为20%

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目

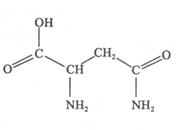
 ,下列叙述正确的有
,下列叙述正确的有  的熔点(填>、=或<),其原因是 。
的熔点(填>、=或<),其原因是 。