题目内容
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中,_______(填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有_______种。
(3)H2S和H2Se的参数对比见下表。
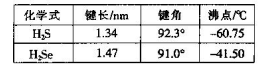
①H2Se的晶体类型为_________,含有的共价键类型为_________。
②H2S的键角大于H2Se的原因可能为____________________。
(4)已知铝(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示
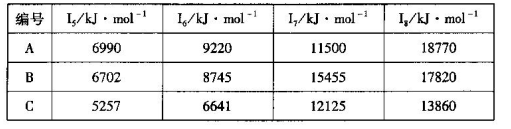
A是____________(填元素符号),B的价电子排布式为 。

(1)天冬酰胺所含元素中,_______(填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有_______种。
(3)H2S和H2Se的参数对比见下表。

①H2Se的晶体类型为_________,含有的共价键类型为_________。
②H2S的键角大于H2Se的原因可能为____________________。
(4)已知铝(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示

A是____________(填元素符号),B的价电子排布式为 。
(1)氮
(2)2
(3)①分子晶体 极性键 ②由于S的电负性强于Se,形成的共用电子对斥力大,键角大;
(4)Mn 3d54s1
试题分析:(1)天冬酰胺含有的H、C、N、O分别有1、2、3、2个没成对电子;(2)碳原子全形成碳碳单键为sp3杂化,有1个碳碳双键的为sp2杂化,故有2种杂化方式;(3)①H2S和H2Se的熔沸点均较低为分子晶体,不同中元素形成的为极性键;②S的电负性强于Se,形成的共用电子对斥力大,键角大;(4)钼、铬、锰价电子数为6、6、7,根据电离能判断得出A、B、C分别有7、6、6个价电子,B的相同级别的电离能大于C,所以B为铬;A为锰;铬的价电子排布式为3d54s1.

练习册系列答案
相关题目
 键
键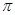 键
键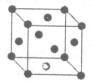
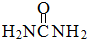 )中
)中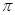 键与
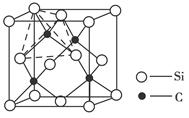
键与 键数目之比为__________;尿素分子中处于同一平面的原子最多有_______个。
键数目之比为__________;尿素分子中处于同一平面的原子最多有_______个。
 、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形;
、④HCHO,其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形;