题目内容
【题目】有A、B、C、D、E五种原子序数增大的元素,只有一种为金属。A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A;B与D同主族;E为第4周期副族元素,其价层电子为全满。
(1)E元素的名称为________,该元素基态原子的价电子排布式为_______。
(2)B与D分别与氢形成最简单氢化物沸点高低顺序为____(用化学式表示);原因_____。
(3)A、B、C三种元素分别与氢形成化合物中的M-M(M代表A、B、C)单键的键能如下表:
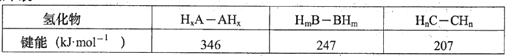
上述三种氢化物中,A、B、C元素原子的杂化方式有_____种;请解释上表中三种氢化物M-M单键的键能依次下降的原因______________________。
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,请写出该条件下DC15电离的电离方程式__________;该熔体中阴离子的空间构型为________。
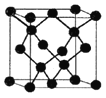
(5)E与C形成的化合物晶体结构有四种,其中一种与金刚石类似,金刚石晶体结构如图所示,该晶体的化学式为______(用元素符号表示);该晶胞的棱长为apm 则该晶体的密度为______g/cm3。
【答案】锌 3d104s2 NH3>PH3 均为分子晶体,NH3分子间存在氢键。 1 乙烷中的碳原子没有孤电子对,肼中的氮原子有1对孤对电子,过氧化氢中的氧原子有两对孤对电子,孤对电子数越多斥力越大,形成的化学键越不稳定,键能越小。 2PCl5=PC16-+PC14 + 正八面体 ZnO ![]()
【解析】
有A、B、C、D、E五种原子序数增大的元素,只有一种为金属,A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A,则A、B、C分别是C、N、O元素;B与D同主族,则D为P元素;E为第4周期副族元素,其价层电子为全满,则为Zn元素;
(1)E为Zn元素,其原子核外3d、4s电子为其价电子;
(2)B与D分别与氢形成最简单氢化物分别是NH3和PH3,含有氢键的氢化物熔沸点高于不含氢键的氢化物;
(3)这几种氢化物中每个M原子价层电子对个数都是4,所以其杂化方式相同;排斥力:孤电子对与孤电子对>孤电子对与成键电子对>成键电子对与成键电子对,排斥力越大,形成的化学键越不稳定;
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定D-Cl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,该阳离子应该为PCl4+,生成的阴离子为PCl6-,利用价层电子对互斥理论判断该阴离子空间构型;
(5)该晶胞中Zn原子个数=4、O原子个数![]() ,根据原子个数比确定化学式;该晶胞体积=(a×10-10 )3cm3,晶胞密度
,根据原子个数比确定化学式;该晶胞体积=(a×10-10 )3cm3,晶胞密度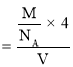 。
。
有A、B、C、D、 E五种原子序数增大的元素,只有一种为金属,A、B、C均为第二周期紧邻元素,其第一电离能顺序为B>C>A,则A、B、C分别是C、N、O元素;B与D同主族,则D为P元素;E为第4周期副族元素,其价层电子为全满,则为Zn元素;
(1)E为Zn元素,其原子核外3d、4s电子为其价电子,其价电子排布式为3d104s2,
故答案为:锌;3d104s2;
(2)B与D分别与氢形成最简单氢化物分别是NH3和PH3,含有氢键的氢化物熔沸点高于不含氢键的氢化物,NH3中含有氢键、PH3中不含氢键,所以熔沸点NH3>PH3,
故答案为:NH3>PH3;均为分子晶体,NH3分子间存在氢键;
(3)这几种氢化物中每个M原子价层电子对个数都是4,所以其杂化方式相同,则杂化方式为一种;排斥力:孤电子对与孤电子对>孤电子对与成键电子对>成键电子对与成键电子对,排斥力越大,形成的化学键越不稳定,乙烷中的碳原子没有孤电子对,肼中的氮原子有1对孤对电子,过氧化氢中的氧原子有两对孤对电子,孤对电子数越多斥力越大,形成的化学键越不稳定,键能越小,
故答案为:1;乙烷中的碳原子没有孤电子对,肼中的氮原子有1对孤对电子,过氧化氢中的氧原子有两对孤对电子,孤对电子数越多斥力越大,形成的化学键越不稳定,键能越小;
(4)D与氯形成的化合物DC15,加压条件下148℃液化,发生完全电离得到一种能够导电的熔体,测定DCl键长为198pm和206pm两种,该熔体中含有一种正四面体结构的阳离子,该阳离子应该为PCl4+,生成的阴离子为PCl6-,其电离方程式为![]() ,
,
该阴离子中P原子价层电子对个数=6+![]() =6,所以为正八面体;
=6,所以为正八面体;
故答案为:![]() ;正八面体;
;正八面体;
(5)该晶胞中Zn原子个数=4、O原子个数=8×18+6×12=4,根据原子个数比确定化学式为ZnO;
该晶胞体积=(a×1010)3cm3,晶胞密度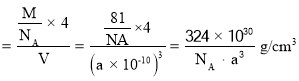 。
。
故答案为:ZnO;![]() 。
。

【题目】用如图所示装置检验乙烯时不需要虚线框中除杂装置的是( )
选项 | 乙烯的制备 | 试剂X | 试剂Y |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | I2的CCl4溶液 |
C | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | I2的CCl4溶液 |
A.AB.BC.CD.D
【题目】甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知 ①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH= + 93.0kJ·mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③甲醇的燃烧热为726.51kJ·mol-1。
要写出表示甲醇燃烧热的热化学方程式,还缺少的热化学方程式为________________。
(2)甲醇可采用煤的气化、液化制取(CO+2H2CH3OH ΔH<0)。在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与![]() 的关系如图所示。
的关系如图所示。
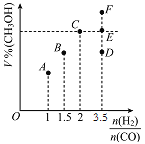
①当起始![]() =2,经过5min达到平衡,0~5min内平均反应速率v(H2)=0.1molL-1min-1,则该条件CO的平衡转化率为_____;若其它条件不变,在T2℃(T2>T1)下达到平衡时CO的体积分数可能是____(填标号)
=2,经过5min达到平衡,0~5min内平均反应速率v(H2)=0.1molL-1min-1,则该条件CO的平衡转化率为_____;若其它条件不变,在T2℃(T2>T1)下达到平衡时CO的体积分数可能是____(填标号)
A.<![]() B.=
B.=![]() C.
C.![]() ~
~ ![]() D.=
D.=![]() E.>
E.> ![]()
②当![]() =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的____点选填“D”、“E”或“F”)。
=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的____点选填“D”、“E”或“F”)。
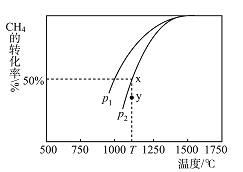
(3)制甲醇的CO和H2可用天然气来制取:CO2(g)+CH4(g)2CO(g)+2H2(g)。在某一密闭容器中有浓度均为0.1mol·L1的CH4和CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则该反应的ΔH______(选填“大于”“小于”或“等于”)0。压强p1_______(选填“大于”或“小于”)p2。当压强为p2时,在y点:v(正)__________(选填“大于”“小于”或“等于”)v(逆)。若p2=6Mpa,则T℃时该反应的平衡常数Kp=_____MPa2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)研究表明:CO2和H2在一定条件下也可以合成甲醇,反应方程式为CO2(g)+3H2(g)CH3OH(g)+H2O(g) [反应Ⅰ]。
①一定条件下,往2L恒容密闭容器中充入2.0mol CO2和4.0mol H2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如下图所示,其中活化能最高的反应所用的催化剂是____(填“A”、“B”或“C”)。

②在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应CO2(g)+H2(g)CO(g)+H2O(g)[反应Ⅱ]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得实验数据:
T(K) | CO2实际转化率(%) | 甲醇选择性(%) |
543 | 12.3 | 42.3 |
553 | 15.3 | 39.1 |
注:甲醇的选择性是指发生反应的CO2中转化为甲醇的百分比。
表中数据说明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是_________。
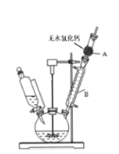
【题目】三苯甲醇(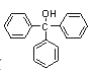 )是重要的有机合成中间体。实验室中合成三苯甲醇时采用如图所示的装置,其合成流程如图:
)是重要的有机合成中间体。实验室中合成三苯甲醇时采用如图所示的装置,其合成流程如图:
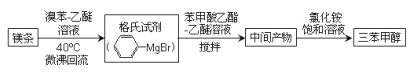
已知:①格氏试剂易潮解,生成可溶于水的 Mg(OH)Br。
②三苯甲醇可通过格氏试剂与苯甲酸乙酯按物质的量比2:1反应合成
③相关物质的物理性质如下:
物质 | 相对分子量 | 沸点 | 熔点 | 溶解性 |
三苯甲醇 | 260 | 380℃ | 164.2℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
乙醚 | - | 34.6℃ | -116.3℃ | 微溶于水,溶于乙醇、苯等有机溶剂 |
溴苯 | - | 156.2℃ | -30.7℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
苯甲酸乙酯 | 150 | 212.6℃ | -34.6℃ | 不溶于水 |
请回答下列问题:
(1)合成格氏试剂:实验装置如图所示,仪器A的名称是____,已知制备格氏试剂的反应剧烈放热,但实验开始时常加入一小粒碘引发反应,推测I2的作用是____。使用无水氯化钙主要是为避免发生____(用化学方程式表示)。
(2)制备三苯甲醇:通过恒压滴液漏斗往过量的格氏试剂中加入13mL苯甲酸乙酯(0.09mol)和15mL无水乙醚的混合液,反应剧烈,要控制反应速率除使用冷水浴外,还可以 ___(答一点)。回流0.5h后,加入饱和氯化铵溶液,有晶体析出。
(3)提纯:冷却后析出晶体的混合液含有乙醚、溴苯、苯甲酸乙酯和碱式溴化镁等杂质,可先通过 ___(填操作方法,下同)除去有机杂质,得到固体17.2g。再通过 ___纯化,得白色颗粒状晶体16.0g,测得熔点为164℃。
(4)本实验的产率是____(结果保留两位有效数字)。本实验需要在通风橱中进行,且不能有明火,原因是____。