题目内容
【题目】日常生活中,汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①2CO(g)+O2(g) ![]() 2CO2(g) ΔH= -akJ/mol
2CO2(g) ΔH= -akJ/mol
②N2(g)+O2(g) ![]() 2NO(g) ΔH= +bkJ/mol
2NO(g) ΔH= +bkJ/mol
③2NO(g)+O2(g) ![]() 2NO2(g) ΔH= -ckJ/mol
2NO2(g) ΔH= -ckJ/mol
回答下列问题:
(1)CO的燃烧热为____________________。
(2)CO将NO2还原为单质的热化学方程式为_____________________________。
(3)为了模拟反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前2s内的平均反应速率V(N2)=_________________________________。
②能说明上述反应达到平衡状态的是_______________。
A.2n(CO2)=n(N2)
B.混合气体的平均相对分子质量不变
C.气体密度不变
D.容器内气体压强不变
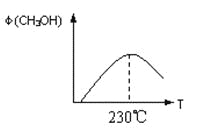
③当NO与CO浓度相等时,体系中NO的平衡转化率与温度、压强的关系如图所示。

则NO的平衡转化率随温度升高而减小的原因是______________________________
图中压强(P1、P2、P3)的大小顺序为_____________________。
【答案】![]() kJ/mol 2NO2(g)+4CO(g)
kJ/mol 2NO2(g)+4CO(g) ![]() N2(g)+4CO2(g) ΔH=-(2a+b-c)kJ/mol 1.875×10-4mol·L-1·s-1 BD 该反应正反应放热,升高温度,平衡逆向移动,NO的平衡转化率减小 P1>P2>P3
N2(g)+4CO2(g) ΔH=-(2a+b-c)kJ/mol 1.875×10-4mol·L-1·s-1 BD 该反应正反应放热,升高温度,平衡逆向移动,NO的平衡转化率减小 P1>P2>P3
【解析】
(1)根据燃烧热的概念进行计算;(2)根据盖斯定律进行分析推导;(3)根据速率计算公式进行计算;(4)根据化学反应达到平衡的条件进行判断化学反应是否达到平衡状态;(5)根据温度和压强对化学反应平衡的影响进行分析。
(1)CO的燃烧热为1molCO完全燃烧生成CO2时放出的热量,所以由①2CO(g)+O2(g) ![]() 2CO2(g) ΔH= -akJ/mol可知,CO(g)+
2CO2(g) ΔH= -akJ/mol可知,CO(g)+![]() O2(g)
O2(g) ![]() CO2(g) ΔH= -
CO2(g) ΔH= -![]() kJ/mol,所以CO的燃烧热为
kJ/mol,所以CO的燃烧热为![]() kJ/mol;答案:
kJ/mol;答案:![]() kJ/mol;
kJ/mol;
(2)由①2CO(g)+O2(g) ![]() 2CO2(g) ΔH= -akJ/mol;②N2(g)+O2(g)
2CO2(g) ΔH= -akJ/mol;②N2(g)+O2(g) ![]() 2NO(g) ΔH= +bkJ/mol; ③2NO(g)+O2(g)2NO2(g) ΔH= -ckJ/mol ,将①
2NO(g) ΔH= +bkJ/mol; ③2NO(g)+O2(g)2NO2(g) ΔH= -ckJ/mol ,将①![]() 2-(②+③)得CO将NO2还原为单质的热化学方程式为4CO(g)+ 2NO2(g)
2-(②+③)得CO将NO2还原为单质的热化学方程式为4CO(g)+ 2NO2(g) ![]() 4CO2(g) + N2(g) ΔH=-2 akJ/mol-(bkJ/mol -ckJ/mol)=-(2a+b-c)kJ/mol;答案:2NO2(g)+4CO(g)
4CO2(g) + N2(g) ΔH=-2 akJ/mol-(bkJ/mol -ckJ/mol)=-(2a+b-c)kJ/mol;答案:2NO2(g)+4CO(g) ![]() N2(g)+4CO2(g) ΔH=-(2a+b-c)kJ/mol;
N2(g)+4CO2(g) ΔH=-(2a+b-c)kJ/mol;
(3)①在2s内,△c(N2)=![]() △c(NO)=
△c(NO)=![]() (10-2.5)
(10-2.5)![]() 10-4 mol·L-1=3.75
10-4 mol·L-1=3.75![]() 10-4 mol .L-1 ,故v(N2)=
10-4 mol .L-1 ,故v(N2)=![]() =img src="http://thumb.1010pic.com/questionBank/Upload/2020/11/11/06/eb9fda86/SYS202011110602134907994150_DA/SYS202011110602134907994150_DA.008.png" width="45" height="41" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />10-4mol·L-1= 1.875
=img src="http://thumb.1010pic.com/questionBank/Upload/2020/11/11/06/eb9fda86/SYS202011110602134907994150_DA/SYS202011110602134907994150_DA.008.png" width="45" height="41" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />10-4mol·L-1= 1.875![]() 10-4 mol·L-1·s-1;答案:1.875
10-4 mol·L-1·s-1;答案:1.875![]() 10-4 mol·L-1·s-1;
10-4 mol·L-1·s-1;
②A.反应物只有NO和CO,根据2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)中,化学计量数之比等于物质的变化量之比,所以在整个反应过程中,一定存在n(CO2) = 2n(N2) ,不能说明化学反应达到平衡状态了, 故A错误;
N2(g)+2CO2(g)中,化学计量数之比等于物质的变化量之比,所以在整个反应过程中,一定存在n(CO2) = 2n(N2) ,不能说明化学反应达到平衡状态了, 故A错误;
B. 由2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)可知,当混合气体的平均相对分子质量不变时,气体物质的量不变,说明混合气体各组分的物质的量不再改变,可以说明反应达到平衡,故B正确;
N2(g)+2CO2(g)可知,当混合气体的平均相对分子质量不变时,气体物质的量不变,说明混合气体各组分的物质的量不再改变,可以说明反应达到平衡,故B正确;
C.气体的密度![]() =
=![]() ,根据质量守恒定律,气体质量不变,容器的体积不变,则气体密度在整个反应过程中始终不变,所以气体密度不变不能作为化学反应达到平衡状态的依据,故C错误;;
,根据质量守恒定律,气体质量不变,容器的体积不变,则气体密度在整个反应过程中始终不变,所以气体密度不变不能作为化学反应达到平衡状态的依据,故C错误;;
D. 由2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)可知,该反应为气体体积减小的反应,故随着反应进行,容器内气体体积减少,压强减小,当压强不变时,说明气体各组分保持平衡不再改变,可以说明反应达到平衡,故D正确;;
N2(g)+2CO2(g)可知,该反应为气体体积减小的反应,故随着反应进行,容器内气体体积减少,压强减小,当压强不变时,说明气体各组分保持平衡不再改变,可以说明反应达到平衡,故D正确;;
综上所述,本题正确答案为BD。
③该反应的正反应放热,升高温度,平衡逆向移动, NO的平衡转化率减小;由方程式2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)可知,正反应为气体体积减小的反应, 相同温度下,增大压强,平衡正向移动,NO的平衡转化率增大,故P1> P2 > P3;
N2(g)+2CO2(g)可知,正反应为气体体积减小的反应, 相同温度下,增大压强,平衡正向移动,NO的平衡转化率增大,故P1> P2 > P3;
答案:该反应正反应放热,升高温度,平衡逆向移动,NO的平衡转化率减小 ; P1>P2>P3。

 阅读快车系列答案
阅读快车系列答案