题目内容
15.在化学反应X+2Y→R+2M 中,已知R和M的摩尔质量之比为22:9,当1.6克X与Y恰好完全反应后,生成4.4克R,则Y与M的质量依次为6.4g、3.6g,解答此题时使用到的化学定律是质量守恒定律.分析 任何化学反应中都遵循质量守恒定律,根据方程式知,该反应中生成R、M的物质的量之比为1:2,R和M的摩尔质量之比为22:9,则生成4.4克R时同时生成M质量=$\frac{4.4g}{22}×2×9$=3.6g,根据质量守恒定律计算Y质量,据此分析解答.
解答 解:任何化学反应中都遵循质量守恒定律,根据方程式知,该反应中生成R、M的物质的量之比为1:2,R和M的摩尔质量之比为22:9,则生成4.4克R时同时生成M质量=$\frac{4.4g}{22}×2×9$=3.6g,根据质量守恒定律得Y质量=4.4g+3.6g-1.6g=6.4g,故答案为:6.4g、3.6g;质量守恒定律.
点评 本题考查化学方程式有关计算,明确各个物理量关系是解本题关键,侧重考查学生分析计算能力,易错点是M质量的计算,题目难度不大.

练习册系列答案
相关题目
12.室温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 饱和氯水中Cl-、NO3-、Na+、SO32- | B. | 在碱性溶液中CO32-、K+、SO42-、Br- | ||
| C. | Na2S溶液中SO42-、K+、Cl-、Cu2+ | D. | pH=12的溶液中NO3-、I-、Na+、Al3+ |
6.在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g),所得实验数据如下表,下列说法正确的是( )
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
| A. | 实验①中,若5min 时测得 n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol/min | |
| B. | 实验②中,该反应的平衡常数K=2.0 | |
| C. | 实验③中,达到平衡时,X的转化率为60% | |
| D. | 实验④中,达到平衡时,b>0.060 |
3.下列物质:(1)Na(2)石墨(3)Na2O (4)SO2 (5)CO2 (6)SO3 (7)NH3•H2O (8)H2S (9)HCl (10)H2SO4 (11)Ba(OH)2 (12)熔融的NaCl (13)蔗糖 (14)NaCl溶液.属于电解质的有
( )
( )
| A. | (3)(7)(9)(10)(11)(12) | B. | (3)(7)(9)(10)(11)(14) | C. | (3)(7)(8)(9)(10)(11)(12) | D. | (1)(3)(7)(8)(9)(10)(11)(12) |
10.把石灰石浸入盐酸中,下列措施能使反应速率增大的是( )
①加大盐酸用量 ②增大盐酸浓度 ③粉碎石灰石 ④增大体系压强.
①加大盐酸用量 ②增大盐酸浓度 ③粉碎石灰石 ④增大体系压强.
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ③④ |
20. 某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.
某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.
为探究其成分,进行了以下实验:
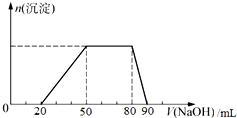
探究一:取10mL该混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示.
探究二:取1L该混合溶液,向该溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示.
下列说法中错误的是( )
 某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.
某混合溶液中,一定含有Cl-、Br-、I-,可能含有的离子如下表所示.| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | CO32-、AlO2-、NO3- |
探究一:取10mL该混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示.
探究二:取1L该混合溶液,向该溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示.
| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n(Cl-) | 2.5mol | 3.0mol | 4.0mol |
| n(Br-) | 3.0mol | 2.8mol | 1.8mol |
| n(I-) | X mol | 0 | 0 |
| A. | X=0.3 | |
| B. | 溶液中n(Cl-):n(Br-):n(I-)=10:15:4 | |
| C. | 加入的氢氧化钠溶液的浓度为1.45mol•L-1 | |
| D. | 溶液中大量存在的离子共有六种 |
7.短周期元素X、Y、Z在周期表中的位置如图所示,则下列说法正确的是( )


| A. | Z一定是活泼的金属 | |
| B. | Y的最高价氧化物的水化物是一种强酸 | |
| C. | Z的最高价氧化物的水化物是强酸 | |
| D. | 1molY单质跟足量水反应时,有3 mol电子发生转移 |
4.如表中评价合理的是( )
| 选项 | 化学反应及其离子方程式 | 评 价 |
| A | NaHSO4溶液与Ba(OH)2溶液反应至 SO42-沉淀完全: 2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | 正 确 |
| B | 向碳酸镁溶液中加入足量稀盐酸: CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
| C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色: Fe3++3H2O=Fe(OH)3↓+3H+ | 正 确 |
| D | NaOH溶液中通入少量CO2反应:OH-+CO2=HCO3- | 正 确 |
| A. | A | B. | B | C. | C | D. | D |