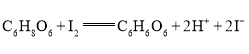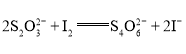题目内容
【题目】人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题:
(1)已知分子式为C6H6的有机物有多种,其中的两种为:(Ⅰ)![]() (Ⅱ)
(Ⅱ)![]() 。
。
①这两种结构的区别表现在以下两方面:
定性方面(即化学性质方面):(Ⅱ)能发生的反应___(填字母),而(Ⅰ)不能。
a.被高锰酸钾酸性溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
定量方面(即消耗反应物的量的方面):
1molC6H6与H2加成时:(Ⅰ)需要H2__mol,而(Ⅱ)需要H2__mol。
②今发现C6H6还可能有一种如图![]() 所示的立体结构,该结构的二氯代物有__种。
所示的立体结构,该结构的二氯代物有__种。
(2)如图是制取溴苯的装置,试回答:
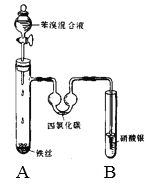
①装置A中发生反应的化学方程式是:____。
②装置B中盛有硝酸银溶液,实验中看到的现象是:___,证明有___生成,说明反应属于___反应(填写反应类型)。
③反应完毕后,将具支试管中的混合液倒入装有水的烧杯中,然后加___溶液后,可除去了其中的溴。写出除溴的化学方程式:___。
④苯易取代,难加成。请写出苯发生硝化反应的方程式:____。
【答案】ab 3 2 3 ![]() +Br2
+Br2![]()
![]() +HBr 淡黄色沉淀 AgBr 取代反应 NaOH Br2+2NaOH→NaBr+NaBrO+H2O
+HBr 淡黄色沉淀 AgBr 取代反应 NaOH Br2+2NaOH→NaBr+NaBrO+H2O ![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
【解析】
(1)根据结构中的官能团分析性质及反应时的数值。
(2)根据苯和溴的反应可能的产物的性质分析反应类型。根据溴和氢氧化钠反应分析产物中溴的除去试剂。
(3)根据苯和硝酸的反应书写方程式。
(1)(Ⅰ)结构中不含碳碳双键,(Ⅱ)含有碳碳双键。①(Ⅱ)能被酸性高锰酸钾溶液氧化,能和溴水发生加成反应,而(Ⅰ)不能。(Ⅰ)需要H23mol,而(Ⅱ)需要H22mol;②![]() 的二氯代物有3种,如图
的二氯代物有3种,如图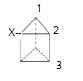 。
。
(2)①苯和溴反应生成溴苯和溴化氢,方程式为:![]() +Br2
+Br2![]()
![]() +HBr ; ②B中有硝酸银,若溶液中有溴化银淡黄色沉淀生成,说明该反应生成溴化氢;说明该反应为取代反应;
+HBr ; ②B中有硝酸银,若溶液中有溴化银淡黄色沉淀生成,说明该反应生成溴化氢;说明该反应为取代反应;
③溴可以和氢氧化钠反应生成溴化钠、次溴酸钠和水,所以用氢氧化钠除去溴,方程式为:Br2+2NaOH→NaBr+NaBrO+H2O;
④苯和浓硝酸在浓硫酸存在下加热反应生成硝基苯和水,方程式为: ![]() +HNO3
+HNO3![]()
![]() +H2O。
+H2O。

【题目】(1)乙醇的分子式是C2H6O。由于有机物普遍存在同分异构现象,其结构简式可能为:
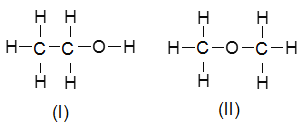
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠及必要的仪器,请同学直接利用如图给定装置开始进行实验确定乙醇的结构。

某同学得到一组实验数据:
乙醇的物质的量(mol) | 氢气的体积(L) |
0.10 | 1.12(标准状况) |
根据以上数据判断乙醇的结构是为____(I、II),理由为____。
(2)某实验小组用下列装置进行乙醇催化氧化的实验。

①实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式_____、____。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是____反应。
②甲和乙两个水浴作用不相同。甲的作用是___;乙的作用是_____。
③反应进行一段时间后,干燥管a中能收集到不同的物质,它们是___。集气瓶中收集到的气体的主要成分是___。
④若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有___。要除去该物质,可在混合液中加入___(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过____(填实验操作名称)即可除去。
【题目】过二硫酸钠(Na2S2O8)也叫高硫酸钠,可用于废气处理及有害物质氧化降解.用(NH4)2S2O8溶液和一定浓度的NaOH溶液混合可制得Na2S2O8晶体,同时还会放出氨气。某化学兴趣小组利用该原理在实验室制备Na2S2O8晶体(装置如图所示).

已知:反应过程中发生的副反应为2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
(1)图中装有NaOH溶液的仪器的名称为___,反应过程中持续通入氮气的目的是___。
(2) (NH4)2S2O8可由电解硫酸铵和硫酸的混合溶液制得,写出电解时阳极的电极反应式:___。
(3)Na2S2O8溶于水中,会发生一定程度的水解,最终仅生成H2SO4、Na2SO4和另一种常温下为液态且具有强氧化性的物质,写出该反应的化学方程式:___。
(4)Na2S2O8具有强氧化性,该兴趣小组设计实验探究不同环境下Na2S2O8氧化性的强弱。将MnSO4H2O(1.69g)与过量Na2S2O8(10g)溶于水中形成的混合溶液煮沸3min,观察并记录加入试剂时和加热过程中的现象(如表格所示)。
环境 | 调节溶液氧化环境时的现象 | 加热煮沸3min期间产生的现象 |
中性 | 加入VmL蒸馏水,无明显现象 | 30s时开始有大量气泡冒出,3min后溶液变深棕色,溶液中有悬浮小颗粒 |
碱性 | 加入VmL某浓度的NaOH溶液,瞬间变为棕色(MnO2) | 10s后溶液逐渐变为深紫色(MnO4-),没有明显冒气泡现象 |
酸性 | 加入VmL稀H2SO4无明显现象 | 煮沸3min后,有气泡冒出 |
①在___(填“中性”“酸性”或“碱性”)条件下,Na2S2O8的氧化能力最强。
②中性氧化时,会产生大量气泡,其原因为___。
③若用0.1molL-1的H2O2溶液滴定碱性氧化反应后的溶液(先将溶液调至酸性再滴定),滴定终点时的现象为___;达到滴定终点时,消耗H2O2溶液的体积为V1rnL。则碱性氧化后的溶液中NaMnO4的质量为___ g(用含V1的代数式表示,5H2O2~2![]() )。
)。