题目内容
下列实验操作及现象都正确,但与新制氯水中某些成分没有关系的是( )
| 序号 | 实验操作 | 现象 | 新制氯水成分 |
| A | 将CaCO3固体加入新制氯水中 | 有无气泡 | HClO |
| B | 红色布条放入新制氯水中 | 使红色布条褪色 | HClO |
| C | 向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液 | 溶液呈血红色 | Cl2 |
| D | 向新制氯水中滴加KI溶液 | 有固体析出 | Cl2 |
| A、A | B、B | C、C | D、D |
考点:氯气的化学性质
专题:卤族元素
分析:氯气与水反应,发生Cl2+H2O=H++Cl-+HClO,氯水中含有HClO、Cl2,具有氧化性,其中HClO具有漂白性,含有H+,具有酸性,以此解答.
解答:
解:A.氯水显酸性,能与碳酸钙反应生成CO2气体,与H+有关,与HClO无关,故A选;
B.次氯酸具有强氧化性,能氧化有色布条,与HClO有关,故不B选;
C.是氯气氧化了亚铁离子,再滴加KSCN溶液,溶液变为血红色,故C不选;
D.是氯气氧化了碘离子生成碘,故D不选.
故选A.
B.次氯酸具有强氧化性,能氧化有色布条,与HClO有关,故不B选;
C.是氯气氧化了亚铁离子,再滴加KSCN溶液,溶液变为血红色,故C不选;
D.是氯气氧化了碘离子生成碘,故D不选.
故选A.
点评:本题考查氯气的性质,侧重于氯水的组成和性质的考查,为高频考点,难度大不,注意把握相关物质的性质.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
A、B、C、D、E、F为原子序数依次增大的短周期元素,其中A与E同主族,B和F同主族,E与F同周期.已知常温下A与E组成的单质状态不同,D的核电荷数是B的最外层电子数2倍,由F组成的单质是一种重要的半导体材料.下列说法不正确的是( )
| A、C的氢化物与C的最高价氧化物的水化物能发生化合反应 |
| B、元素的非金属性由强到弱的顺序是:D>C>B>F |
| C、原子半径由大到小的顺序是:E>F>C>D |
| D、F与D形成的化合物性质很不活泼,不与任何酸反应 |
下列叙述正确的是( )
| A、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| B、铜片加入氯化铁溶液中发生反应:3Cu+2Fe3+=3Cu2++2Fe |
| C、FeCl2、Fe(OH)3、Cu2S均可通过化合反应制得 |
| D、在pH=1溶液中,NH4+、K+、ClO-、Cl-可以大量共存 |
下列有关的离子方程式中正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4+ | ||||
B、铜片接电源正极,碳棒接电源负极,电解硫酸溶液Cu+2H+
| ||||
| C、磷酸一氢钠溶液水解:HPO42-+H2O═PO43-+H3O+ | ||||
| D、实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O═4Fe3++4OH- |
下列说法正确的是( )
| A、其他条件不变加水稀释,醋酸的电离平衡向右移动,醋酸的电离平衡常数增大 | ||
| B、向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全的离子方程式为:Al3++SO42-+Ba2++30H-═BaSO4↓+Al(OH)3↓ | ||
| C、0.2mol?L-1的某一元弱酸HA溶液和0.1mol?L-1 NaOH溶液等体积混合后的溶液:2c(0H-)+c(A-)=2c(H+)+c(HA) | ||
D、已知
|
下列离子方程式中,正确的是( )
| A、铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、碳酸镁与稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
| C、大理石与盐酸反应:CO32-+2H+═CO2↑+H2O |
| D、稀硫酸与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
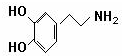 快乐是什么?专家通过实验发现:在大脑的相应部位--“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态.人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.多巴胺结构如图:
快乐是什么?专家通过实验发现:在大脑的相应部位--“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态.人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.多巴胺结构如图: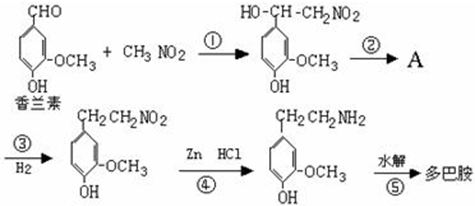
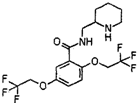 ,它可由龙胆酸(
,它可由龙胆酸(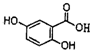 ,为原料合成,合成的方法如图:
,为原料合成,合成的方法如图: