题目内容
下列离子方程式中,正确的是( )
| A、铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、碳酸镁与稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
| C、大理石与盐酸反应:CO32-+2H+═CO2↑+H2O |
| D、稀硫酸与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.铁与稀硫酸反应生成硫酸亚铁和氢气,不会生成铁离子;
B.碳酸镁与稀硫酸反应生成硫酸镁、二氧化碳气体和水,碳酸镁需要保留化学式;
C.大理石为难溶物,在离子方程式中碳酸钙不能拆开,需要保留化学式;
D.稀硫酸与氢氧化钡反应生成硫酸钡沉淀和水,漏掉了氢离子与氢氧根离子的反应.
B.碳酸镁与稀硫酸反应生成硫酸镁、二氧化碳气体和水,碳酸镁需要保留化学式;
C.大理石为难溶物,在离子方程式中碳酸钙不能拆开,需要保留化学式;
D.稀硫酸与氢氧化钡反应生成硫酸钡沉淀和水,漏掉了氢离子与氢氧根离子的反应.
解答:
解:A.铁与稀硫酸反应生成亚铁离子和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故A错误;
B.碳酸镁与稀硫酸反应生成硫酸镁、二氧化碳和水,反应的离子方程式为:MgCO3+2H+═Mg2++H2O+CO2↑,故B正确;
C.大理石为碳酸钙,与盐酸反应生成氯化钙、二氧化碳和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故C错误;
D.稀硫酸与氢氧化钡溶液反应,漏掉了氢离子与氢氧根离子反应生成水的反应,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选B.
B.碳酸镁与稀硫酸反应生成硫酸镁、二氧化碳和水,反应的离子方程式为:MgCO3+2H+═Mg2++H2O+CO2↑,故B正确;
C.大理石为碳酸钙,与盐酸反应生成氯化钙、二氧化碳和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故C错误;
D.稀硫酸与氢氧化钡溶液反应,漏掉了氢离子与氢氧根离子反应生成水的反应,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选B.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
下列反应中硝酸既表现氧化性,又表现酸性的是( )
| A、氧化铝和硝酸 |
| B、氧化铜和硝酸 |
| C、硫化氢和硝酸 |
| D、铜和浓硝酸 |
根据酸碱质子理论判定下列说法不正确的是( )
| A、所有的弱酸根都是碱 |
| B、酸式弱酸根既是酸又是碱 |
| C、不可能一种物质既是酸又是碱 |
| D、氢氧根是碱 |
决定化学反应速率的主要因素是( )
| A、催化剂 |
| B、参加反应的物质本身的性质 |
| C、反应物的浓度 |
| D、温度、压强以及反应物的接触面 |
下列叙说正确的是( )
| A、一定温度下,若等浓度的NaA,NaB溶液,pH前者大于后者,则HA,HB的Ka前者小于后者 |
| B、在一定温度下的CaSO4的水溶液中,Ca2+和SO42-浓度的乘积是一定是常数 |
| C、常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为3c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3) |
D、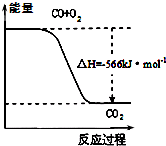 已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ?mol-1图可表示由CO生成CO2的反应过程和能量关系 |
下列说法中,正确的是( )
| A、冰醋酸是弱电解质,液态时能导电 |
| B、强电解质溶液的导电能力不一定比弱电解质强 |
| C、盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱 |
| D、电解质达到电离平衡后,各种离子的浓度相等 |
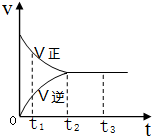 如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应X2+3Y2?2Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( )| A、t1时,只有正方向反应 |
| B、t2时,反应到达限度 |
| C、t2-t3,反应不再发生 |
| D、t2-t3,各物质的浓度不再发生变化 |
元素周期表中,划分周期的依据是( )
| A、元素的核电荷数 |
| B、元素原子的电子层数 |
| C、元素的化合价 |
| D、元素原子的最外层电子数 |