题目内容
17.由铜片、锌片和200mL稀H2SO4组成的原电池中,若锌片发生电化学腐蚀,则当铜片上放出3.36L(标态)气体时,硫酸恰好全部作用完.试计算:(1)产生这些气体消耗了多少克锌
(2)有多少个电子通过了导线
(3)200mL稀H2SO4的物质的量浓度是多少.
分析 该原电池中,锌电极上电极反应式为Zn-2e-=Zn2+,铜电极上电极反应式为2H++2e-=H2↑,则电池反应式为Zn+2H+=H2↑+Zn2+,
(1)根据氢气和锌之间的关系式计算锌的质量;
(2)根据氢气和转移电子之间的关系式计算转移电子的物质的量;
(3)根据氢原子守恒计算硫酸的浓度.
解答 解:该原电池中,锌电极上电极反应式为Zn-2e-=Zn2+,铜电极上电极反应式为2H++2e-=H2↑,则电池反应式为Zn+2H+=H2↑+Zn2+,
(1)设参加反应的Zn的质量为x,
Zn+2H+=H2↑+Zn2+
65g 22.4L
x 3.36L
则x=$\frac{65g×3.36L}{22.4L}$=9.75g
答:消耗锌的质量9.75g;
(2)设转移电子的物质的量为y,
Zn+2H+=H2↑+Zn2+转移电子
22.4L 2mol
3.36L y
y=$\frac{3.36L×2mol}{22.4L}$=0.30mol,
答:通过电子的物质的量为0.30mol;
(3)根据氢原子守恒得H2SO4~H2,则c(H2SO4)=$\frac{\frac{3.36L}{22.4L/mol}}{0.2L}$=0.75 mol•L-1,
答:原硫酸的浓度为0.75 mol•L-1.
点评 本题以原电池原理为载体考查了物质的量的有关计算,根据各个物理量之间的关系来分析解答,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
7.某原电池的总反应是:Zn+Cu2+═Zn2++Cu,此反应的原电池的正确组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Cu | Zn | HCl |
| B | Zn | Cu | CuSO4 |
| C | Cu | Zn | CuSO4 |
| D | Cu | Zn | ZnCl2 |
| A. | A | B. | B | C. | C | D. | D |
5.下列说法正确的是( )
| A. | 用BaCl2 溶液可证明Na2CO3溶液显碱性时由于CO32-发生水解 | |
| B. | NaHCO3 溶液中存在:c(Na+ )=c(HCO3-)+c(CO3 2-) | |
| C. | CH3COOH溶液中加入少量CH3COONa 固体后溶液中c(H+)•c(CH3COO-)增大 | |
| D. | 相同温度下,Ksp较小的物质其溶解度也一定较小 |
12.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | C4H10 | C. | CH2Cl2 | D. | C2H4Cl2 |
9.下列电子式书写正确的是( )
| A. | OH- | B. | 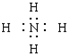 | C. | 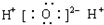 | D. |  |
6.下列烷烃的一氯代物中没有同分异构体的是( )
| A. | 丁烷 | B. | 丙烷 | C. | 乙烷 | D. | 2-甲基丙烷 |
7.下列表示丙基的是( )
| A. | CH3CH2CH3 | B. | CH3CH2CH2- | C. | -CH2CH2- | D. | CH3- |

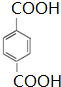 .
. +2Br2$\stackrel{光照}{→}$
+2Br2$\stackrel{光照}{→}$ +2HBr.?
+2HBr.? $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$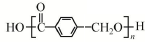 +(n-1)H2O.
+(n-1)H2O. .
.