��Ŀ����
5�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺
��1����ͼ1��1mol NO2��1mol CO��Ӧ����CO2��NO�����������仯ʾ��ͼ��ͼ���漰���ʾ�Ϊ��̬������д��NO2��CO��Ӧ���Ȼ�ѧ����ʽNO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ•mol-1��
��2����0.5L���ܱ������У�����һ�����ĵ������������з�Ӧ��������������ʵ�����ʱ��ı仯������ͼ2��ʾ����Y��H2��2min��N2�ķ�Ӧ���ʦԣ�N2��=0.1mol•L-1•min-1��
��3�����Ṥҵ�ڹ��á�������ҵ�ͺ�����ҵ��ռ����Ҫ��λ�����Ż�ѧ��ά�������л��ϳɡ�����������ȹ�ҵ��Ѹ�ٷ�չ����Ҫʹ�ô��������ᣮ
�ٹ�ҵ�������ò�ϵ������Ϊ�������ð���������ȡ���ᣮ��һ����ӦΪ���ڴ���������������������Ӧ����NO��д����Ӧ��ѧ����ʽ4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O��
��ͭ������ϡ���ᷴӦ��Ҳ����Ũ���ᷴӦ����ͭ��һ��Ũ�����ᷴӦʱ���ɽ�����ʽ��ʾΪ��Cu+HNO3��Cu��NO3��2+NO��+NO2��+H2O������ʽδ��ƽ������Ӧ�л�ԭ������NO��NO2��0��.6mol Cu��������ȫ�ܽ������õ���NO��NO2���ʵ�����ͬ����õ���״�����������Ϊ13.44L��
���� ��1��������˷�Ӧ���ʱ䣬�����Ȼ�ѧ����ʽ����д������д���Ȼ�ѧ����ʽ��
��2�����ݵ����������ķ�Ӧ֮�ȣ���֪YΪ���������ݻ�ѧ��Ӧ���ʼ��㹫ʽ������
��3���Ʊ�����ĵ�һ����Ӧ�ǰ��Ĵ���������һ��������ˮ�����ݻ��ϼ۷�����ԭ������ݵ����غ��������������
��� �⣺��1���÷�Ӧ���ʱ��H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol���ʴ�Ϊ��NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ•mol-1��
��2�����ݵ����������ķ�Ӧ֮�ȣ���֪YΪ������2min��N2�ķ�Ӧ���ʦԣ�N2��=$\frac{��c}{��t}$=$\frac{0.1mol}{0.5L��2min}$=0.1mol•L-1•min-1���ʴ�Ϊ��H2��0.1mol•L-1•min-1��
��3���Ʊ�����ĵ�һ����Ӧ�ǰ��Ĵ���������һ��������ˮ����4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O�������еĵ�Ԫ�ػ��ϼ۽��ͣ���NO��NO2Ϊ��ԭ�������õ���NO��NO2���ʵ�����ͬ�������Ϊ1mol����Ԫ�صĵ�����Ϊ4������һ�μӷ�Ӧ��ͭ�����ʵ���Ϊ2mol��0.6mol Cu��������ȫ�ܽ������0.3mol��һ��������0.3mol������������õ���״�����������Ϊ22.4L/mol��0.6mol=13.44L���ʴ�Ϊ����4NH3+5O2$\frac{\underline{����}}{��}$4NO+6H2O����NO��NO2��13.44��
���� ���⿼���Ȼ�ѧ����ʽ����д�����ݷ�Ӧ����������������Ĵ�С�����Ӧ�ȣ��Ѷ��еȣ�

| A�� | ˮ | B�� | CCl4 | C�� | ��ˮ | D�� | ˮ�� |
��1����֪����Fe2O3+3C��ʯī��s��=2Fe��s��+3CO��g����H1=+489.0kJ•mol-1��C��ʯī��s��+CO2��g��=2CO��g����H2=+172.5kJ•mol-1��a=-28.5kJ•mol-1��
��2��ұ������Ӧ��ƽ�ⳣ������ʽK=$\frac{{c}^{3}��C{O}_{2}��}{{c}^{3}��CO��}$���¶����ߺ�Kֵ��С������������䡱��С������
��3����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�ĺ����ܱ����������У��ֱ��������ʾ���ݼ������ʣ���Ӧ����һ��ʱ���ﵽƽ�⣮
| Fe2O3 | CO | Fe | CO2 | |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 2.0 | 1.0 | 1.0 |
������˵����ȷ����AB������ĸ��
a�������������ܶȺ㶨ʱ����־��Ӧ�ﵽƽ��״̬
b����������CO��ƽ��ת���ʴ����ҵ�
c���ס����������У�CO��ƽ��Ũ��֮��Ϊ2��3
d������Fe2O3�����������CO��ת����
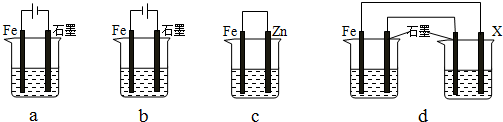
��4����ȡһ����ʩ�ɷ�ֹ������ʴ������װ���е��ձ���ʢ�е�Ũ�ȡ��������NaCl��Һ��
����a��cװ���У��ܱ���������bc������ĸ����
������dװ�ñ�������X���ĵ缫����Ӧ��п�������ƣ���
| A�� | ��� �ܣ��٣��ڣ��� | B�� | �ܶ� �٣��ܣ��ۣ��� | ||
| C�� | ���� �ܣ��٣��ۣ��� | D�� | ��ԭ���� �ڣ��ܣ��ۣ��� |
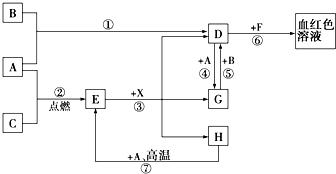 A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ������£�AΪ���壬BΪҺ�壬CΪ���壮D��E��F��G��H��X��Ϊ���������X��һ������ǿ�ᡢEΪ��ɫ���壬H�ڳ�����ΪҺ�壮����֮���ת����ϵ��ͼ��ʾ������ijЩ��Ӧ�����Ͳ��ַ�Ӧ��������ȥ����
A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ������£�AΪ���壬BΪҺ�壬CΪ���壮D��E��F��G��H��X��Ϊ���������X��һ������ǿ�ᡢEΪ��ɫ���壬H�ڳ�����ΪҺ�壮����֮���ת����ϵ��ͼ��ʾ������ijЩ��Ӧ�����Ͳ��ַ�Ӧ��������ȥ���� 2013��12��15��4ʱ���س���ϵ�л���ġ����úš�˳��ʻ��������棬ʵ�������Ǻ���ҫ����Ĵ��٣����������Ҫ����ȼ�ϣ�ͨ�����£�N2H4����ȼ�ϣ�N2O4������������ش��������⣺
2013��12��15��4ʱ���س���ϵ�л���ġ����úš�˳��ʻ��������棬ʵ�������Ǻ���ҫ����Ĵ��٣����������Ҫ����ȼ�ϣ�ͨ�����£�N2H4����ȼ�ϣ�N2O4������������ش��������⣺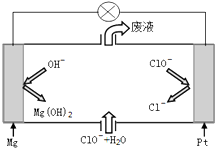 ��������Ҫ���Եز�����ʣ���������ơ�����þ����̬���ڣ�����������������Ҫ��Ӧ�ã�
��������Ҫ���Եز�����ʣ���������ơ�����þ����̬���ڣ�����������������Ҫ��Ӧ�ã�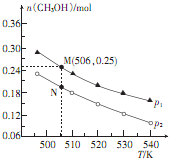 ����Ȼ��Ϊԭ�Ϻϳɼ״������ķ�����ˮú����Ŀǰ���ڿ�����ֱ��������
����Ȼ��Ϊԭ�Ϻϳɼ״������ķ�����ˮú����Ŀǰ���ڿ�����ֱ��������