题目内容
13.高炉炼铁是冶炼铁的主要方法,发生的主要反应为Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=a kJ•mol-1.(1)已知:①Fe2O3+3C(石墨,s)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1②C(石墨,s)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1则a=-28.5kJ•mol-1.
(2)冶炼铁反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,温度升高后,K值减小(填“增大”、“不变”或“减小”).
(3)在T℃时,该反应的平衡常数K=64,在2L的恒容密闭容器甲和乙中,分别按照如表所示数据加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |
②下列说法正确的是AB(填字母)
a.容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙两容器中,CO的平衡浓度之比为2:3
d.增加Fe2O3的量可以提高CO的转化率
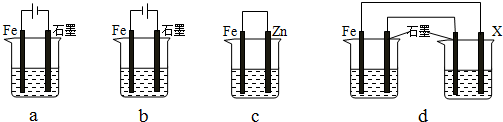
(4)采取一定措施可防止钢铁腐蚀.下列装置中的烧杯里盛有等浓度、等体积的NaCl溶液.
①在a~c装置中,能保护铁的是bc(填字母).
②若用d装置保护铁,X极的电极材料应是锌(填名称).
分析 (1))①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJmol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJmol-1
①-②×3得到Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g),依据热化学方程式和盖斯定律计算;
(2)Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1依据平衡常数概念写出表达式,反应是吸热反应,升温平衡逆向进行;
(3)①在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲中,加入物质反应达到平衡,依据平衡三段式列式计算结合转化率概念计算得到;
②Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1
A.反应前后气体质量变化,体积不变,若容器内气体密度恒定时,标志反应达到平衡状态;
B.乙容器中一氧化碳增加,相当于增大压强,反应前后体积不变,甲容器中CO的平衡转化率等于乙的转化率,速率甲小于乙;
C.依据平衡三段式计算平衡物质的量;计算甲、乙容器中,CO的平衡浓度之比;
D.固体量增加不影响化学平衡,增加Fe2O3不能提高CO的转化率.
(4)①原电池的正极和电解池的阴极可以得到保护;
②装置为原电池,若用d装置保护铁,X极的电极材料应比铁活泼.
解答 解:(1)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJmol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJmol-1
由盖斯定律①-②×3得到Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1,故答案为:-28.5;
(2)Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1,平衡常数K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$;反应是放热反应,升温平衡逆向进行,平衡常数减小,
故答案为:$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$;减小;
(3)①在T℃时,该反应的平衡常数K=64,在2L恒容密闭容器甲中,加入物质反应达到平衡,设消耗一氧化碳物质的量为x
Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)
起始量(mol) 1 1 1 1
变化量(mol) x x
平衡量(mol) 1-x 1+x
K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$=$\frac{(1+x)^{3}}{(1-x)^{3}}$=64,计算得到x=0.6
转化率=60%,故答案为:60%;
②Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJmol-1
A.反应前后气体质量变化,体积不变,若容器内气体密度恒定时,标志反应达到平衡状态,故A正确;
B.乙容器中一氧化碳增加,将乙中CO用K=64,代入三段式计算求得CO减少了1.7mol,故CO的转化率为$\frac{1.7}{2.0}$×100%=70%,反应速率乙大,故B正确;
C.甲容器中平衡一氧化碳物质的量为0.4mol;乙容器中结合平衡常数计算得到消耗一氧化碳为1.4mol,平衡物质的量为0.6mol,甲和乙容器中CO的平衡浓度之比为0.4+0.6=2:3;故C错误;
D.固体量增加不影响化学平衡,增加Fe2O3不能提高CO的转化率,故D错误;
故答案为:AB;
(4)①装置中原电池的正极和电解池的阴极可以得到保护,a中Fe作阳极被腐蚀,b中Fe作阴极被保护,c中Fe作正极被保护,则bc可以保护铁,故答案为:bc;
②装置为原电池,若用d装置保护铁,X极的电极材料应比铁活泼可以选择锌,故答案为:锌.
点评 本题考查了热化学方程式和盖斯定律计算应用,平衡常数计算应用,化学平衡三段式列式计算方法,题目难度中等.

(1)工业冶炼铝,以石墨为阳极.阳极反应式为2O2--4e-=O2↑,可能发生副反应有C+O2$\frac{\underline{\;高温\;}}{\;}$CO2(或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO).
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为CO-2e-+H2O=CO2+2H+
(3)向75mL 4mol•L-1KOH溶液中缓慢通入4480mL CO2气体(标准状况)恰好完全被吸收.
①写出该反应的离子方程式:2CO2+3OH-=CO32-+HCO3-+H2O.
②该吸收溶液中离子浓度大小排序为c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
③常温下,a mol•L-1KHCO3溶液的pH=8,HCO3-的水解常数约等于$\frac{1{0}^{-12}}{a-1{0}^{-6}}$.(用含a式表示).
(4)已知:①2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③CO(g)+2H2(g)?CH3OH(g)△H3=-90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H=-763.8kJ•mol-1.
(5)某温度下,发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.0kJ•mol-1
①向某容器中充入1.0mol H2O和1.0mol CO (g),在一定条件下发生上述反应.混合气体中CO的物质的量与时间关系如下列所示:
| 0 | 5min | 10min | 15min | 20min | 25min | |
| Ⅰ(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| Ⅱ(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应.
下列图象正确且说明可逆反应达到平衡状态的是A.(填序号)

| A. | 标准状况下22.4L Cl2与足量NaOH溶液反应生成NaCl和NaClO,转移电子数为Na | |
| B. | 16g甲烷中含有的非极性共价键键数为4Na | |
| C. | 一定两点额SO2溶于水后形成pH为2的水溶液,其中H+的数目为0.01Na | |
| D. | 1.8gD2O中含有的质子数为2Na |
 完成下列各题:
完成下列各题:(1)已知下列反应的热化学方程式:
①6C (s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1;
②2H2(g)+O2 (g)=2H2O(g)△H2;
③C(s)+O2(g)═CO2(g)△H3.
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为12△H3+5△H2-2△H1.
(2)向体积为10L的恒容密闭容器中通入3mol X,在一定温度下发生如下反应:2X(g)?Y(g)+az(g),经5min后反应达到反应限度(即达到平衡状态).
①平衡时,测得容器内的压强为起始时的1.2倍,此时X的物质的量浓度为0.24mol•L-1,则方程式中a=3;用Y表示的反应速率为0.006mol•L-1•min-1.
②若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一时间内测得容器内的反应速率如表所示:
| 容器 | 反应速率 | 容器 | 反应速率 |
| 甲 | v(X)=3.5mol•L-1•min-1 | 乙 | v(Y)=2 mol•L-1•min-1 |
| 丙 | v(Z)=4.5mol•L-1•min-1 | 丁 | v(X)=0.075mol•L-1•s-1 |
(3)高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.
①则阳极的电极反应式为:Fe-6e-+8OH-=FeO42-+4H2O;
②若隔膜为阴离子交换膜,则OH-自左向右移动(填左、右):
③假设电解前后体积变化忽略不计,撤去隔膜混合后,与原溶液比较pH降低(升高、降低或不变)
 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.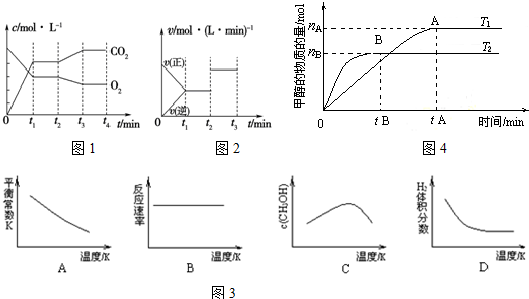

 A、B、C、D、E是中学常见的五种物质,其转化关系如图所示.其中某些物质可能已略去.已知D是单质,C、E是化合物.
A、B、C、D、E是中学常见的五种物质,其转化关系如图所示.其中某些物质可能已略去.已知D是单质,C、E是化合物. ;
;