ЬтФПФкШн
ЁОЬтФПЁПЫцзХЕЭЬМИжЕШНрОЛИжММЪѕЕФЗЂеЙЃЌ![]() ФЭЛ№ВФСЯКЭИжЫЎжЎМфЕФЯрЛЅзїгУвбГЩЮЊЕБЧАЕФвЛИібаОПжиЕуЁЃ
ФЭЛ№ВФСЯКЭИжЫЎжЎМфЕФЯрЛЅзїгУвбГЩЮЊЕБЧАЕФвЛИібаОПжиЕуЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉШеГЃЩњЛюжаТСгУЦЗБШЬњЦїМўИќФЭИЏЪДЃЌдвђЪЧ________ЁЃ
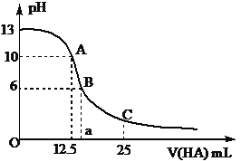
ЃЈ2ЃЉдкТёЬПЪЕбщЬѕМўЯТЃЌВЛЭЌЬМЫиВФСЯЕФ![]() ФЭЛ№ВФСЯгыЬњвКжЎМфЕФПЩФмЗДгІШчЯТЃК
ФЭЛ№ВФСЯгыЬњвКжЎМфЕФПЩФмЗДгІШчЯТЃК
Ђй![]()
![]() ЃЛ
ЃЛ
Ђк![]()
![]() ЃЛ
ЃЛ
Ђл![]()
![]() ЃЛ
ЃЛ
дђ![]() ЕФ
ЕФ![]() ______
______![]() ЁЃ
ЁЃ
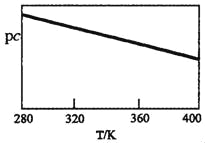
ЃЈ3ЃЉЪЕбщЮТЖШЯТЃЌ(![]() )/FeЯЕЭГжаДцдкзХЯрЛЅЗДгІЃЌШч
)/FeЯЕЭГжаДцдкзХЯрЛЅЗДгІЃЌШч![]() ШмШыЬњвКжаЃЌЕМжТЬњвКжаЦНКтЕФТСЕФАйЗжКЌСПЕФЖдЪ§(lg[Al])КЭЦНКтбѕ(
ШмШыЬњвКжаЃЌЕМжТЬњвКжаЦНКтЕФТСЕФАйЗжКЌСПЕФЖдЪ§(lg[Al])КЭЦНКтбѕ(![]() )ЕФАйЗжКЌСПЕФЖдЪ§(lg[
)ЕФАйЗжКЌСПЕФЖдЪ§(lg[![]() ])ЙиЯЕШчЭМЫљЪОЃЌЭМжаЮТЖШ
])ЙиЯЕШчЭМЫљЪОЃЌЭМжаЮТЖШ![]() ___1973K(ЬюЁА>ЁБЛђЁА<ЁБ).
___1973K(ЬюЁА>ЁБЛђЁА<ЁБ).

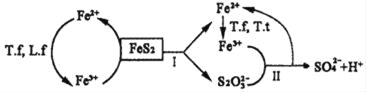
ЃЈ4ЃЉдкТёЬПЧщПіЯТЃЌЬМЙ§ЪЃЪБЃЌЬМЕФбѕЛЏЗДгІжївЊПМТЧЃК![]() ЁЃдкЪЕбщЪвбаОПИУЗДгІЃЌвЛЖЈЮТЖШЯТ.ЯђФГЬхЛ§ПЩБфЕФКубЙУмБеШнЦї(змбЙЧПЮЊ
ЁЃдкЪЕбщЪвбаОПИУЗДгІЃЌвЛЖЈЮТЖШЯТ.ЯђФГЬхЛ§ПЩБфЕФКубЙУмБеШнЦї(змбЙЧПЮЊ![]() )МгШызуСПЕФЬМКЭ1mol
)МгШызуСПЕФЬМКЭ1mol![]() ЃЌЦНКтЪБЬхЯЕжаЦјЬхЬхЛ§ЗжЪ§гыЮТЖШЕФЙиЯЕШчЭМЫљЪОЃК
ЃЌЦНКтЪБЬхЯЕжаЦјЬхЬхЛ§ЗжЪ§гыЮТЖШЕФЙиЯЕШчЭМЫљЪОЃК

Ђй650ЁцЪБЃЌИУЗДгІДяЕНЦНКтКѓЮќЪеЕФШШСПЪЧ_____ЃЌЧхКФЬМЕФжЪСПЮЊ____ЁЃ
ЂкTЁцЪБЃЌШєЯђЦНКтЬхЯЕжадйГфШывЛЖЈСПвдV![]() )ЃКV(
)ЃКV(![]() )=5ЃК4ЕФЛьКЯЦјЬхЃЌЦНКт___(ЬюЁАЯђе§ЗДгІЗНЯђЁБЁАЯђФцЗДгІЗНЯђЁБЛђЁАВЛЁБ)вЦЖЏЁЃ
)=5ЃК4ЕФЛьКЯЦјЬхЃЌЦНКт___(ЬюЁАЯђе§ЗДгІЗНЯђЁБЁАЯђФцЗДгІЗНЯђЁБЛђЁАВЛЁБ)вЦЖЏЁЃ
Ђл925ЁцЪБЃЌгУЦНКтЗжбЙДњЬцЦНКтХЈЖШБэЪОЕФЛЏбЇЦНКтГЃЪ§![]() =__[гУКЌ
=__[гУКЌ![]() ЕФДњЪ§ЪНБэЪОЃЌЦјЬхЗжбЙ(
ЕФДњЪ§ЪНБэЪОЃЌЦјЬхЗжбЙ(![]() )=ЦјЬхзмбЙ(
)=ЦјЬхзмбЙ(![]() )XЬхЛ§ЗжЪ§]ЁЃ
)XЬхЛ§ЗжЪ§]ЁЃ
ЃЈ5ЃЉCOПЩзїФГШлШкбЮЕчГиЕФШМСЯЃЌЕчНтжЪЮЊ![]() КЭ
КЭ![]() ЕФШлШкбЮЛьКЯЮяЃЌПеЦјгы
ЕФШлШкбЮЛьКЯЮяЃЌПеЦјгы![]() ЕФЛьКЯЦјЮЊжњШМЦјЃЌЕчГидк650ЁцЯТЙЄзїЪБЃЌИКМЋЕФЕчМЋЗДгІЪНЮЊ________ЁЃ
ЕФЛьКЯЦјЮЊжњШМЦјЃЌЕчГидк650ЁцЯТЙЄзїЪБЃЌИКМЋЕФЕчМЋЗДгІЪНЮЊ________ЁЃ
ЁОД№АИЁПТСгУЦЗБэУцЮЊвЛВужТУмЕФ![]() БЁФЄЃЌзшжЙТСЕФНјвЛВНбѕЛЏ -681.5 < 43.125kJ 3.0g Яђе§ЗДгІЗНЯђ 23.04
БЁФЄЃЌзшжЙТСЕФНјвЛВНбѕЛЏ -681.5 < 43.125kJ 3.0g Яђе§ЗДгІЗНЯђ 23.04![]()
![]()
ЁОНтЮіЁП
(1).ШеГЃЩњЛюжаТСгУЦЗБШЬњЦїМўИќФЭИЏЪДЃЌжївЊдвђЪЧвђЮЊТСжЦЦЗБэУцгавЛВужТУмЕФбѕЛЏФЄ![]() БЁФЄЃЌПЩзшжЙТСЕФНјвЛВНбѕЛЏЃЌЙЪД№АИЮЊТСгУЦЗБэУцЮЊвЛВужТУмЕФ
БЁФЄЃЌПЩзшжЙТСЕФНјвЛВНбѕЛЏЃЌЙЪД№АИЮЊТСгУЦЗБэУцЮЊвЛВужТУмЕФ![]() БЁФЄЃЌзшжЙТСЕФНјвЛВНбѕЛЏЃЛ
БЁФЄЃЌзшжЙТСЕФНјвЛВНбѕЛЏЃЛ
(2).НЋЬѕМўЪННјааБрКХЃЌРћгУИЧЫЙЖЈТЩевГіФПБъЪНгыЬѕМўЪНЕФЙиЯЕЃК
Ђй![]()
![]() ЃЛ
ЃЛ
Ђк![]()
![]() ЃЛ
ЃЛ
Ђл![]()
![]() ЃЛ
ЃЛ
дђ![]() ЕФ
ЕФ![]() Ђй/2-3Ђл/2+3Ђк/2= -681.5
Ђй/2-3Ђл/2+3Ђк/2= -681.5![]()
ЙЪД№АИЮЊ-681.5![]() ЃЛ
ЃЛ
(3). ДгЭМжаПЩПДГіЃЌЕБТСЕФАйЗжКЌСПЕФЖдЪ§(lg[Al])вЛЖЈЪБЃЌ![]() ЪБЕФЦНКтбѕ(
ЪБЕФЦНКтбѕ(![]() )ЕФАйЗжКЌСПЕФЖдЪ§(lg[
)ЕФАйЗжКЌСПЕФЖдЪ§(lg[![]() ])БШ1973KЪБЕЭЃЌЫЕУїЖдгк
])БШ1973KЪБЕЭЃЌЫЕУїЖдгк![]() етвЛЮќШШЕФПЩФцЗДгІ
етвЛЮќШШЕФПЩФцЗДгІ![]() ЪБЦНКтФцЯђвЦЖЏЃЌЫЕУїЭМжаЮТЖШ
ЪБЦНКтФцЯђвЦЖЏЃЌЫЕУїЭМжаЮТЖШ![]() ЃМ1973KЃЌЙЪД№АИЮЊЃМЃЛ
ЃМ1973KЃЌЙЪД№АИЮЊЃМЃЛ
(4). ЂйДгЭМжаЃЌПЩжЊЕБ650ЁцЪБЃЌЗДгІДяЦНКтЪБВњЮяCOЕФЬхЛ§ЗжЪ§ЮЊ40%ЃЌЩшЗЂЩњЗДгІЕФ![]() ЮяжЪЕФСПЮЊxЃЌСаГіШ§ааЪН
ЮяжЪЕФСПЮЊxЃЌСаГіШ§ааЪН
![]()
![]() ЃЛ
ЃЛ
ЪМ 1mol 0mol
зЊ xmol 2xmol
ЦН 1-xmol 2xmol
ПЩЕУ![]() ЃЌЧѓНтПЩЕУx=0.25molЃЛ
ЃЌЧѓНтПЩЕУx=0.25molЃЛ
ЙЪДЫЪБЗДгІЮќЪеЕФШШСПЮЊ0.25mol![]() 172.5
172.5![]() =43.125kJЃЛ
=43.125kJЃЛ
ЧхКФЬМЕФжЪСПЮЊ12![]() ЁС0.25mol=3gЃЛ
ЁС0.25mol=3gЃЛ
ЙЪД№АИЮЊ43.125kJЁЂ3.0gЃЛ
Ђк ДгЭМжаПЩжЊЃЌTЁцИУЗДгІДяЦНКтЪБЃЌV![]() )%=V(
)%=V(![]() )%ЃЌИУЦНКтЬхЯЕЕФЦНКтГЃЪ§K=1ЁЃШєдйГфШывЛЖЈСПвдV
)%ЃЌИУЦНКтЬхЯЕЕФЦНКтГЃЪ§K=1ЁЃШєдйГфШывЛЖЈСПвдV![]() )ЃКV(
)ЃКV(![]() )=5ЃК4ЕФЛьКЯЦјЬхЃЌДЫЪБЬхЯЕжаЕФQc=
)=5ЃК4ЕФЛьКЯЦјЬхЃЌДЫЪБЬхЯЕжаЕФQc=![]() ЃМKЃЌЙЪЗДгІНЋЯђе§ЗДгІЗНЯђвЦЖЏЃЌЙЪД№АИЮЊЯђе§ЗДгІЗНЯђвЦЖЏЃЛ
ЃМKЃЌЙЪЗДгІНЋЯђе§ЗДгІЗНЯђвЦЖЏЃЌЙЪД№АИЮЊЯђе§ЗДгІЗНЯђвЦЖЏЃЛ
Ђл 925ЁцЪБЃЌ![]() ЕФЬхЛ§ЗжЪ§ЮЊ96%ЃЌДЫЪБ
ЕФЬхЛ§ЗжЪ§ЮЊ96%ЃЌДЫЪБ![]() ЕФЬхЛ§ЗжЪ§ЮЊ4%ЃЌЫљвдгУЦНКтЗжбЙДњЬцЦНКтХЈЖШБэЪОЕФЛЏбЇЦНКтГЃЪ§
ЕФЬхЛ§ЗжЪ§ЮЊ4%ЃЌЫљвдгУЦНКтЗжбЙДњЬцЦНКтХЈЖШБэЪОЕФЛЏбЇЦНКтГЃЪ§![]() =
= ![]() =23.04
=23.04![]() ЃЌЙЪД№АИЮЊ23.04
ЃЌЙЪД№АИЮЊ23.04![]() ЃЛ
ЃЛ
(5). COзїШМСЯЪБЃЌдкдЕчГиИКМЋЩЯЗЂЩњЗДгІЃЌбѕЛЏВњЮяЮЊ![]() ЃЌДЫЪБЕФЕчНтжЪЮЊ
ЃЌДЫЪБЕФЕчНтжЪЮЊ![]() КЭ
КЭ![]() ЕФШлШкбЮЛьКЯЮяЃЌЙЪИКМЋЕФЕчМЋЗДгІЪНгІаДЮЊ
ЕФШлШкбЮЛьКЯЮяЃЌЙЪИКМЋЕФЕчМЋЗДгІЪНгІаДЮЊ![]() ЃЌЙЪД№АИЮЊ
ЃЌЙЪД№АИЮЊ![]() ЁЃ
ЁЃ