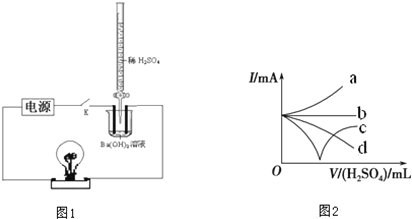
题目内容
向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:____________。在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:________________。2H++S
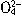 +Ba2++2OH-=2H2O+BaSO4↓; Ba2++ S
+Ba2++2OH-=2H2O+BaSO4↓; Ba2++ S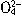 =BaSO4↓
=BaSO4↓【试题分析】
解析:欲使溶液呈中性,只需将H+恰好中和,则其离子方程式为2H++S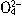 +Ba2++2OH-=2H2O+BaSO4↓。而上述中性溶液中有S
+Ba2++2OH-=2H2O+BaSO4↓。而上述中性溶液中有S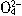 ,继续滴加Ba(OH)2溶液,Ba2+与S
,继续滴加Ba(OH)2溶液,Ba2+与S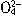 反应生成BaSO4沉淀,则其离子方程式为S
反应生成BaSO4沉淀,则其离子方程式为S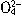 +Ba2+=BaSO4↓。故正确答案为2H++S
+Ba2+=BaSO4↓。故正确答案为2H++S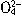 +Ba2++2OH-=2H2O+BaSO4↓;Ba2++
+Ba2++2OH-=2H2O+BaSO4↓;Ba2++
S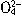 =BaSO4↓。
=BaSO4↓。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目