��Ŀ����
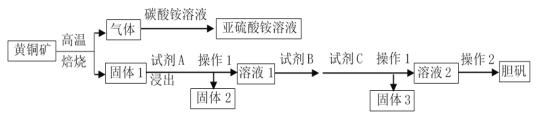
����Ŀ�������ҹ����Ԫ�ء�����ר�Ҿ������ڿ���������2016��Ԫ��ȷ�Ͻ���ʡ�����ش����������������ٿӶ���һ��ȷ���˽���ʡ�������ٶ����ĵ�λ����Ȼ�������в��������٣�+6�ۣ����ε���ʽ���ڡ����ٿ����Ҫ�ɷ��������̵������Σ�FeWO4��MnWO4��������SiO2��Al2O3�����ʡ����ú��ٿ��Ʊ������ٵ�����ͼ��ͼ��
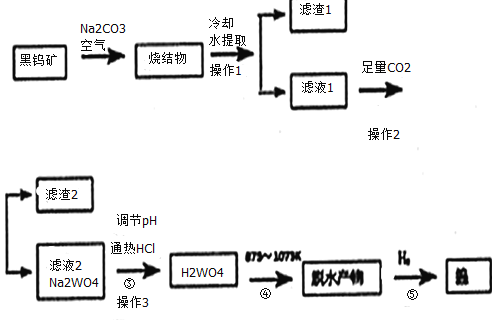
˵����a����Ӧ�����ڸ��������½��еģ��ս���ɷ�Ϊ��Fe2O3��Mn2O4��NaAlO2��Na2SiO3��Na2WO4
b������Fe2O3�ķ�ӦΪ��4FeWO4+4Na2CO3+O2=4Na2WO4+4CO2+2Fe2O3
c����pHֵ3.0��4.4������Һ�У���������������������ʷ��룬���պ�Ϊ��������
�ش��������⣺
��1��д���ս���������Na2SiO3�Ļ�ѧ��Ӧ����ʽ��__������Mn2O4������Fe2O3�������ķ�Ӧԭ����ͬ����д������Mn3O4�Ļ�ѧ��Ӧ����ʽ��___��
��2������3��Ҫ�õ������������У�__��
��3��ͨ������CO2ʱ���������ӷ�Ӧ����ʽΪ��___��___��
��4������������������ٵ��Ʊ����ڹ�ҵұ�������ĺ��ַ���___��
��5���ҹ��ٻ�ѧ�о��ĵ���˹�����������������ķ�Ӧ�Ƶ���һ�ֻ�ɫ�ġ������ȵ��ٵ�������WO��3-x����������ɫ�����پ��бȱ������ԭ���ŵ㡣һ����Ϊ����ɫ�����ٵ���ɫ�ͷ����Ȱ�ʾ���ڻ������д�������ۺ�����������״̬���٣���x��ֵΪ0.1������ɫ�������������ּ�̬����ԭ����֮��Ϊ___��
���𰸡�Na2CO3+SiO2![]() Na2SiO3+CO2�� 6MnWO4+6Na2CO3+O2=6Na2WO4+6CO2+2Mn3O4 ���������ձ���©�� CO2+AlO2-+2H2O=Al��OH��3��+HCO3- 2CO2+SiO32-+2H2O=H2SiO3��+2HCO3- �Ȼ�ԭ�� 1��4
Na2SiO3+CO2�� 6MnWO4+6Na2CO3+O2=6Na2WO4+6CO2+2Mn3O4 ���������ձ���©�� CO2+AlO2-+2H2O=Al��OH��3��+HCO3- 2CO2+SiO32-+2H2O=H2SiO3��+2HCO3- �Ȼ�ԭ�� 1��4
��������
���ٿ����Ҫ�ɷ��������̵������Σ�FeWO4��MnWO4��������SiO2��Al2O3�������ڿ����м��������������ڣ��ս���ɷ�Ϊ��Fe2O3��Mn2O4��NaAlO2��Na2SiO3��Na2WO4����ȴ�ܽ���˵õ���ҺA����pHֵ3.0��4.4������Һ�У����������������B�����ʷ��룬���պ�Ϊ�������٣�������ԭ�����ٵõ������٣��ݴ˷�������
��1��̼���ƺͶ��������ϼ��ȷ�Ӧ���ɹ����ƺͶ�����̼���ս���������Na2SiO3�Ļ�ѧ��Ӧ����ʽΪ��Na2CO3+SiO2![]() Na2SiO3+CO2������Ϸ�Ӧ4FeWO4+4Na2CO3+O2=4Na2WO4+4CO2+2Fe2O3������Mn2O4������Fe2O3�������ķ�Ӧԭ����ͬ�����Ƶõ���MnWO4��Na2CO3������е�������Ӧ����Na2WO4��CO2��Mn3O4����������Mn3O4�Ļ�ѧ��Ӧ����ʽΪ��6MnWO4+6Na2CO3+O2=6Na2WO4+6CO2+2Mn3O4��
Na2SiO3+CO2������Ϸ�Ӧ4FeWO4+4Na2CO3+O2=4Na2WO4+4CO2+2Fe2O3������Mn2O4������Fe2O3�������ķ�Ӧԭ����ͬ�����Ƶõ���MnWO4��Na2CO3������е�������Ӧ����Na2WO4��CO2��Mn3O4����������Mn3O4�Ļ�ѧ��Ӧ����ʽΪ��6MnWO4+6Na2CO3+O2=6Na2WO4+6CO2+2Mn3O4��
��2������3Ϊ������Һ����Ĺ��˲�������Ҫ�õ������������У����������ձ���©����
��3����Һ1��ͨ�����������̼����Һ��ƫ��������Ӻ���������̼��Ӧ������������������̼�����ƣ�ͨ������CO2ʱ���������ӷ�Ӧ����ʽΪ��CO2+AlO2-+2H2O=Al��OH��3��+HCO3-��������̼��������ӷ�Ӧ���ɰ�ɫ�������ᣬ��Ӧ�����ӷ���ʽΪ��2CO2+SiO32-+2H2O=H2SiO3��+2HCO3-��
��4��������֪��H2WO4��ˮ����ΪWO3��ͨ��������ԭ�����ٽ�����WO3+3H2![]() W+3H2O��ұ���ķ��������Ȼ�ԭ����
W+3H2O��ұ���ķ��������Ȼ�ԭ����
��5���ٵ�������WO��3-x����x=0.1�����ٵ�������ΪWO2.9�����������Ϊx�������۵���Ϊ��1-x�������ݻ��ϼ۴����͵���0��5x+6(1-x)=2.9��2,x=0.2������ۺ�����������״̬���ٵı�Ϊ0.2��(1-0.2)=1:4��

����Ŀ������Դ��ѭ��������Ŀǰ�о����ȵ�֮һ��
��1��һ�ֿ��Կ��������İ��������ͼa��ʾ��

��֪��![]()
![]()
�������ⷴӦ��![]() ��
��![]() ��__
��__![]()
��2��1100��ʱ������˿����NH3�ֽ�İ�˥��(Ũ�ȼ�Сһ������ʱ��)���±���ʾ��
c(NH3)/mol/L | 4.56��10-3 | 2.28��10-3 | 1.14��10-3 | 5.70��10-4 | 2.85��10-4 |
ʱ��/s | 0 | 440 | 660 | 770 | t5 |
���е�t5��ֵΪ_________��c(NH3)��ֵ��4.56��10��3�仯��2.28��10��3�Ĺ����У�ƽ����Ӧ������v(H2)=_____________ (������λ��Ч����)mol��L��1��S��1��
��3����101kPa�£�NH3�ֽ��ƽ��ת�������¶ȵĹ�ϵ��ͼb��ʾ��
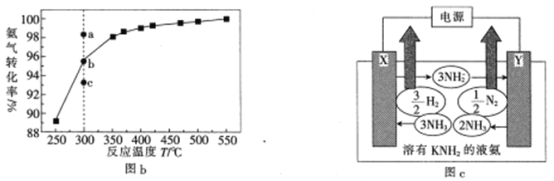
���¶�Ϊ300�棬��ѹΪ101kPaʱ��ͼb��v(��)>v(��)�ĵ���_____(�a����b����c��)��
��Ϊ����NH3�ֽ�Ļ�ܿɲ�ȡ�Ĵ�ʩ��_____________________________
��4����֪Һ���д�������ƽ�⣺2NH3(l)![]() NH4����NH2���������н�������������(��KNH2)��Һ��������ʵ������Ĺ���ԭ����ͼc��ʾ��
NH4����NH2���������н�������������(��KNH2)��Һ��������ʵ������Ĺ���ԭ����ͼc��ʾ��
�ٵ缫X��������__________________(���������������)��
��ͼc�������ĵ缫��ӦʽΪ______________________________________________
����ͼc��֧�ֵ���ʸ���NH4Cl���������ĵ缫��ӦʽΪ__________________________