题目内容
【题目】如图是甲烷(CH4)和白磷(P4)分子的空间结构示意图,请把你认为是化学键的虚线改为实线,把碳原子涂成实心小圆点(在图上改即可__________)。甲烷分子是________(填“左”、“右”)图。从图中看出,每个甲烷分子中有________对共用电子,而白磷分子中形成______个共价键,键角为________。甲烷是由________键(填“极性”或“非极性”,下同)形成的________分子,白磷是由________键形成的________分子。
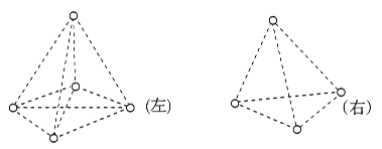
【答案】 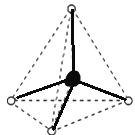 左 4 6 60° 极性 非极性 非极性 非极性
左 4 6 60° 极性 非极性 非极性 非极性
【解析】
甲烷分子是五原子的正四面体,而白磷是四原子的正四面体,每个甲烷分子中碳原子与氢原子形成4对共用电子对,而白磷分子中形成6条P-P键,由此分析解答。
甲烷分子是五原子的正四面体,分子结构为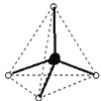 ,而白磷是四原子的正四面体,所以左边是甲烷分子,每个甲烷分子中碳原子与氢原子形成4对共用电子对,而白磷分子中形成6条P-P键,键角为60°。甲烷和白磷均为正四面体结构的分子,其中甲烷是由极性键形成的非极性分子,白磷是由非极性键形成的非极性分子。故答案为:
,而白磷是四原子的正四面体,所以左边是甲烷分子,每个甲烷分子中碳原子与氢原子形成4对共用电子对,而白磷分子中形成6条P-P键,键角为60°。甲烷和白磷均为正四面体结构的分子,其中甲烷是由极性键形成的非极性分子,白磷是由非极性键形成的非极性分子。故答案为: ;左;4;6;60°;极性;非极性;非极性;非极性。
;左;4;6;60°;极性;非极性;非极性;非极性。

 天天练口算系列答案
天天练口算系列答案【题目】今年6月20日,2016年全球最受关注的十大化学成果发布,其中有两项与空气中的二氧化碳处理利用技术有关。其一为美国伊利诺斯大学芝加哥分校和阿贡国家实验室科学家联合设计的新型太阳能电池,可直接把大气中的二氧化碳转化为合成气(CO和H2)该设计同时具有环保和经济价值,不仅可以减缓二氧化碳的排放,而且可以生成重要的化工原料。
(1)下列材料也可以用于制造太阳能电池的是____________。
A.Ag2O B.Fe3O4 C.Si D.SiO2
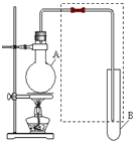
(2)下图装置可实现二氧化碳到一氧化碳的转化
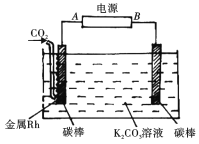
①电源的正极为______(“A”或“B")。
②阴极发生反应的电极方程式为:___________.
(3)CO 和H2可用于合成甲醇。
①已知CO、H2、CH3OH(1)的燃烧热为283.0kJ/mol、285.8kJ/mol、726.5kJ/mol,写出 由CO和H2制备CH3OH(1)的热化学方程式__________。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,发生反应CO(g)+2H2(g) ![]() CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
时间(min) | 0 | 1 | 5 | 10 | 30 | 50 |
压强(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
该温度下的平衡常数是_____。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,CH3OH的体积分数比原平衡时_____( 填“大”或“小”)。