题目内容
18.下列有关化学用语正确的是( )| A. | 乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能为同分异物体 | |
| B. | 北京奥运会奖牌--“金镶玉”奖牌玉的化学成分多为含水钙镁硅酸盐,如:Ca2Mg5Si8O22(OH)2可用氧化物表示为:2CaO•5MgO•8SiO2•H2O | |
| C. | 次氯酸的结构式为:H-Cl-O | |
| D. | 丙烷分子的比例模型示意图: |
分析 A.结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
B.根据化合价书写氧化物形式,一般为格式为:较活泼金属氧化物•较不活泼金属氧化物•二氧化硅•水,注意符合元素的比例关系;
C.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合;
D.比例模型表明原子的比例大小、原子之间的连接形式、空间结构,不能表明原子之间的成键情况.
解答 解:A.乙醇、乙二醇与丙三醇所含羟基的个数不同,不为同系物,故A错误;
B.根据化合价生成氧化物形式,一般为格式为:较活泼金属氧化物•较不活泼金属氧化物•二氧化硅•水,注意符合元素的比例关系,故Ca2Mg5Si8O22(OH)2可用氧化物表示为:2CaO•5MgO•8SiO2•H2O,故B正确;
C.次氯酸是共价化合物,氧原子与氢原子、氯原子分别通过1对共用电子对结合,结构式为H-O-Cl,故C错误;
D.选项中的模型表明原子的比例大小、原子之间成键情况、空间结构,为丙烷的球棍模型,故D错误.
故选B.
点评 本题考查常用化学用语的书写,难度不大,注意区分球棍模型与比例模型,硅酸盐改写为氧化物形式,注意元素的比例关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.四种短周期元素在周期表中的位置如图,其中只有M为金属元素,下列说法不正确的是( )
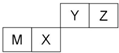

| A. | 原子半径Z<M | |
| B. | Z位于元素周期表中第2周期、第ⅥA族 | |
| C. | X的最简单气态氢化物的热稳定性比Z的小 | |
| D. | X的最高价氧化物不溶于任何酸 |
9.某同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插入浓硫酸,加热;
Ⅱ.待产生黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用.
(1)甲同学认为根据所学知识:已知硫化铜(CuS)、硫化亚铜(Cu2S)、粉末和氧化铜粉末相似且都不溶于水,在空气中煅烧硫化铜和硫化亚铜都转化二种氧化物,设计一个不用任何化学试剂就能鉴别氧化铜、硫化铜、硫化亚铜三种粉末的简便实验方案,请帮助甲同学将方案填写于下表中,实验提供天平及其他必要的设备.
(2)乙同学查阅文献得知检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+.该同学假设黑色沉淀是CuO.检验过程如下:
①将CuO放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色沉淀放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6]溶液,未见红褐色沉淀.
由该检验过程所得结论是黑色沉淀中不含有CuO.
(3)丙同学再次假设,黑色沉淀是铜的硫化物.实验如下:
①现象2说明黑色沉淀具有还原性.
②能确认黑色沉淀中含有S元素的现象是B试管中出现白色沉淀,相应的离子方程式是NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+.
③为确认黑色沉淀是“铜的硫化物”,还需进行的实验操作是取冷却后A装置试管中的溶液,滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+,说明黑色沉淀是铜的硫化物.
以上实验说明,黑色沉淀中存在铜的硫化物.进一步实验后证明黑色沉淀是CuS与Cu2S的混合物.将黑色沉淀放入浓硫酸中加热一段时间后,沉淀溶解,其中CuS溶解的化学方程式是CuS+4H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+4SO2↑+4H2O.
(4)丁同学通过实验确认,固体只含有硫化铜和硫化亚铜,他通过以下实验求硫化亚铜的百分含量:取2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol/L(NH4)2Fe(SO4)2溶液完全反应.
则混合物中Cu2S的质量分数为40%.
Ⅰ.将光亮铜丝插入浓硫酸,加热;
Ⅱ.待产生黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用.
(1)甲同学认为根据所学知识:已知硫化铜(CuS)、硫化亚铜(Cu2S)、粉末和氧化铜粉末相似且都不溶于水,在空气中煅烧硫化铜和硫化亚铜都转化二种氧化物,设计一个不用任何化学试剂就能鉴别氧化铜、硫化铜、硫化亚铜三种粉末的简便实验方案,请帮助甲同学将方案填写于下表中,实验提供天平及其他必要的设备.
| 实验步骤 | 实验现象 | 结论及有关化学方程式 |
| A.分别称取相同质量的样品,在空气中燃烧; B.分别称量硫化铜和硫化亚铜灼烧后剩余物质的质量 | A.有一种固体无变化,两种固体产生刺激性气味气体 B.有一种样品质量减轻,一种样品质量不变 | A.固体无变化的是氧化铜,产生刺激性气味气体的是硫化铜和硫化亚铜,在空气中煅烧中反应的化学方程式分别为2CuS+3O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO+2SO2; Cu2S+2O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2 B.质量减轻的是硫化铜,质量不变的是硫化亚铜 |
①将CuO放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6]溶液,产生红褐色沉淀.
②将黑色沉淀放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6]溶液,未见红褐色沉淀.
由该检验过程所得结论是黑色沉淀中不含有CuO.
(3)丙同学再次假设,黑色沉淀是铜的硫化物.实验如下:
| 实验装置 | 现象 |
 | 1.A试管中黑色沉淀逐渐溶解 2.A试管内上方出现红棕色气体 3.B试管中出现白色沉淀 |
②能确认黑色沉淀中含有S元素的现象是B试管中出现白色沉淀,相应的离子方程式是NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+.
③为确认黑色沉淀是“铜的硫化物”,还需进行的实验操作是取冷却后A装置试管中的溶液,滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+,说明黑色沉淀是铜的硫化物.
以上实验说明,黑色沉淀中存在铜的硫化物.进一步实验后证明黑色沉淀是CuS与Cu2S的混合物.将黑色沉淀放入浓硫酸中加热一段时间后,沉淀溶解,其中CuS溶解的化学方程式是CuS+4H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+4SO2↑+4H2O.
(4)丁同学通过实验确认,固体只含有硫化铜和硫化亚铜,他通过以下实验求硫化亚铜的百分含量:取2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol/L(NH4)2Fe(SO4)2溶液完全反应.
则混合物中Cu2S的质量分数为40%.
13.石墨是层状晶体,每一层内碳原子排列成正六边形,一个个正六边形排列成平面网状结构,如果将每对相邻碳原子间的短线看成一个化学键,则石墨晶体中每一层内碳原子数与C-C键数的比是( )
| A. | 2:3 | B. | 1:3 | C. | 1:1 | D. | 1:2 |
7.实验室配制450mL1.0mol?L-1 NaOH溶液,下列有关说法正确的是( )
| A. | 应用托盘天平称取20g NaOH固体 | |
| B. | 配制过程中所用玻璃棒的作用是搅拌和引流 | |
| C. | NaOH固体在烧杯中称量时间过长,所配NaOH溶液的浓度偏大 | |
| D. | 定容摇匀后,发现液面下降,继续加水至刻度线,对所配NaOH溶液的浓度无影响 |
8.有关硅元素的下列叙述中正确的是( )
| A. | 硅与任何酸都不反应 | |
| B. | 硅是构成矿物岩石的主要原料,其化合态硅几乎全部是硅石(成份为SiO2)和硅酸盐 | |
| C. | 硅的性质很稳定,能以游离态存在于自然界 | |
| D. | 常温时硅不与任何物质反应 |

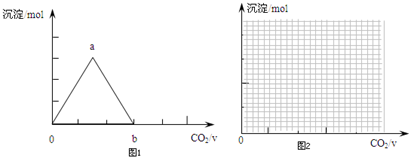
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示 (已知硝酸只被还原为NO气体).
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示 (已知硝酸只被还原为NO气体).