题目内容
【题目】如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
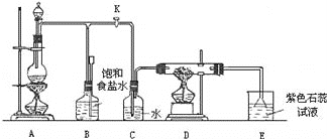
(1)A是氯气发生装置,其中反应的化学方程式为_____。
(2)实验开始时,先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯,连接上E装置。Cl2通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出D中反应的化学方程式:_____。装置C的作用是_____。
(3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是_____。
(4)若将E处烧杯中溶液改为澄清石灰水,反应过程现象为_____(选填标号)。
A.有白色沉淀生成 B.无现象 C.先生成白色沉淀,而后白色沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,此时B中的现象是_____,B的作用是_____。
【答案】4HCl(浓)+MnO2![]() MnCl2+2H2O+Cl2↑ 2Cl2+2H2O(g)+C
MnCl2+2H2O+Cl2↑ 2Cl2+2H2O(g)+C![]() 4HCl↑+CO2↑ 吸收Cl2中的HCl气体,提供D处所需水蒸气 生成的HCl气体使紫色石蕊溶液变红,因未反应完的Cl2与H2O作用产生的HClO的漂白作用使红色消失 B 瓶中液面下降,长颈漏斗内液面上升 贮存少量Cl2
4HCl↑+CO2↑ 吸收Cl2中的HCl气体,提供D处所需水蒸气 生成的HCl气体使紫色石蕊溶液变红,因未反应完的Cl2与H2O作用产生的HClO的漂白作用使红色消失 B 瓶中液面下降,长颈漏斗内液面上升 贮存少量Cl2
【解析】
(1)根据浓盐酸和二氧化锰的性质判断生成物,从而确定方程式;(2)氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应;氯化氢气体极易溶于水,且水能提供水蒸气,据此分析;(3)紫色石蕊试液遇酸变红,但次氯酸有漂白性,据此分析;(4)氯化氢、次氯酸和澄清石灰水反应都生成可溶性的盐和水;(5)根据B装置内气体的压强变化分析液面变化。
(1)浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水,故答案为:4HCl(浓盐酸)+MnO2![]() MnCl2+2H2O+Cl2↑;
MnCl2+2H2O+Cl2↑;
(2)A装置产生了氯气,C装置为D装置提供水蒸气,氯气有强氧化性,碳有还原性,在加热条件下氯气和水、碳发生氧化还原反应生成氯化氢和二氧化碳,反应方程式为:2Cl2+2H2O(气)+C![]() 4HCl↑+CO2↑;盐酸有挥发性,所以制取的氯气中含有氯化氢气体,氯化氢极易溶于水,通过以上分析知,C装置的作用是:吸收Cl2中的HCl气体,提供D处所需水蒸气,故答案为:2Cl2+2H2O(气)+C
4HCl↑+CO2↑;盐酸有挥发性,所以制取的氯气中含有氯化氢气体,氯化氢极易溶于水,通过以上分析知,C装置的作用是:吸收Cl2中的HCl气体,提供D处所需水蒸气,故答案为:2Cl2+2H2O(气)+C![]() 4HCl↑+CO2↑;吸收Cl2中的HCl气体,提供D处所需水蒸气;
4HCl↑+CO2↑;吸收Cl2中的HCl气体,提供D处所需水蒸气;
(3)D装置中生成了HCl和CO2,它们的水溶液呈酸性,剩余的氯气在E装置中和水反应生成盐酸和次氯酸,所以溶液呈酸性,紫色石蕊试液遇酸变红色,次氯酸有漂白性,能使溶液褪色,故答案为:生成的HCl气体使紫色石蕊溶液变红,因未反应完的Cl2与H2O作用产生的HClO的漂白作用使红色消失;
(4)剩余的氯气在E装置中和水反应生成盐酸和次氯酸,氯化氢、次氯酸和澄清石灰水反应都生成可溶性的盐和水,盐酸酸性大于碳酸,所以二氧化碳和氢氧化钙不反应,则反应过程无现象,故答案为:B;
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有Cl2产生,气体通过导管进入B装置,导致B装置中气体的压强增大,大于大气压,迫使瓶中液面下降,长颈漏斗内液面上升;饱和食盐水能抑制氯气的溶解,所以B装置的作用是贮存少量Cl2,故答案为:瓶中液面下降,长颈漏斗内液面上升;贮存少量Cl2。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案