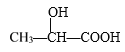题目内容
【题目】某化学实验室需要1.500 mol·L-1硫酸溶液450 mL。根据溶液的配制情况回答下列问题:
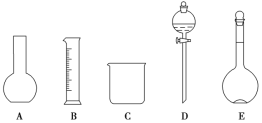
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(2)现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制450 mL 1.50 mol·L-1的稀硫酸。计算所需浓硫酸的体积为________ mL (保留1位小数),现有 ①10 mL ②25 mL ③50 mL ④100 mL四种规格的量筒,最好选用的量筒是________(填代号)。
(3)配制时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为:②→①→③→___→_____→_____→______→④(填序号)。
(4)在配制过程中,下列操作中会导致所配制的溶液浓度偏高的有________。
①用量筒量取浓硫酸时候,俯视刻度线
②洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,俯视刻度线
【答案】AD 璃棒、胶头滴管 40.8 ③ ⑧ ⑤ ⑥ ⑦ ②④
【解析】
(1)根据配制一定物质的量浓度的溶液所需要的仪器进行分析;
(2)根据稀释溶液的公式进行计算,再根据所量取浓硫酸体积选择量筒;
(3)配制一定物质的量浓度的溶液的操作步骤分析;
(4)根据配制溶液的误差判断。
(1)配制步骤有计算、称量(量取)、溶解、冷却、移液、洗涤、定容、摇匀等操作,若溶质为固体,一般用托盘天平称量,用药匙取用药品;若溶质为液体,一般用量筒量取。然后在烧杯中溶解,冷却后转移到相应规格的容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、筒量、玻璃棒、容量瓶、胶头滴管,所以不需要的仪器是AD,还需要的仪器是胶头滴管和玻璃棒。故答案为:AD;玻璃棒、胶头滴管;
(2)配制450 mL 1.50 mol·L-1的稀硫酸,因实验室没有450 mL规格的容量瓶,必须配制500 mL 1.50 mol·L-1的稀硫酸,由于稀释过程中溶质不变,则0.5L![]() 1.50 mol·L-1 =
1.50 mol·L-1 =![]() VL,所以需要浓硫酸的体积是V=0.0408L=40.8mL,所以应该需要50mL量筒,答案选③;
VL,所以需要浓硫酸的体积是V=0.0408L=40.8mL,所以应该需要50mL量筒,答案选③;
(3)配制一定物质的量浓度的溶液的操作步骤有计算、称量(或量取)、溶解(或稀释)、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量(或用量筒量取),用药匙取用药品,在烧杯中溶解(或稀释),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.故正确的操作顺序为:②①③⑧⑤⑥⑦④;
(4)①用量筒量取浓硫酸时候,俯视刻度线,所量取的浓硫酸体积偏少,配得溶液浓度偏低;
②洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中,所取浓硫酸的量偏多,配得溶液浓度偏高;
③转移前,容量瓶中含有少量蒸馏水,定容时需要加入蒸馏水,故对所酸溶液的浓度无影响;
④定容时,俯视刻度线,所加蒸馏水的体积偏小,所配溶液的浓度偏高;
答案选②④。

 夺冠金卷全能练考系列答案
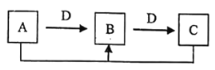
夺冠金卷全能练考系列答案【题目】研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
反应Ⅱ:CH3OCH3(g)+H2O(g)![]() 2CH3OH(g) △H2=+23.4 kJ/mol
2CH3OH(g) △H2=+23.4 kJ/mol
反应Ⅲ:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=____kJ/mol。
(2)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是___(填序号)。
A.反应体系总压强保持不变
B.容器内的混合气体的密度保持不变
C.水分子中断裂2NA个H-O键,同时氢分子中断裂3NA个H-H键
D.CH3OH和H2O的浓度之比保持不变
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如下:
物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
浓度/mol·L-1 | 1.8 | 1.8 | 0.4 |
此时v正___v逆(填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH体积分数(CH3OH)% =___%。
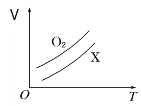
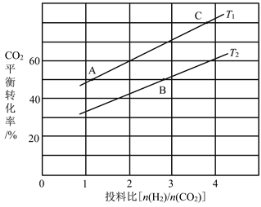
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6mol CO2和12mol H2充入2 L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=____;KA、KB、KC三者之间的大小关系为____。
(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。其中:CH3OH的选择性=![]() ×100%
×100%
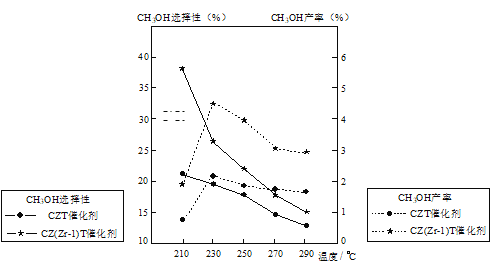
①温度高于230℃,CH3OH产率随温度升高而下降的原因是_____。
②在上述条件下合成甲醇的工业条件是____。
p>A.210℃ B.230℃ C.催化剂CZT D.催化剂CZ(Zr-1)T【题目】下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较金属镁和铝的活泼性 | 分別向两只盛有等体积等浓度的稀硫酸烧杯中加入打磨过的同样大小的镁片和铝片,比较反应现象 |
B | 除去Mg粉中混有的Al 粉 | 加入足量的NaOH 溶液,过滤、洗涤、干燥 |
C | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
D | 配制0.4000mol·L1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,直接向烧杯中加入250mL水 |
A. AB. BC. CD. D