题目内容
【题目】实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收Cu并制备ZnO的部分实验过程如图所示:
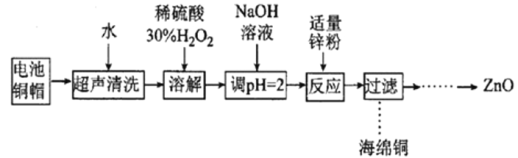
下列叙述错误的是
A. 合理处理废弃旧电池的铜帽既有利于节约资源,又有利于保护环境
B. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2
C. 加入锌粉反应的离子为Cu2+
D. “过滤”操作后直接将溶液蒸发结晶、高温灼烧得到ZnO
【答案】D
【解析】
A.合理处理废弃旧电池中的铜帽,既避免了旧电池造成的污染,又实现了资源的再利用,A项正确;B.在酸性条件下,O2能像H2O2一样,将铜氧化为Cu2+,通常需要加热,反应方程式为:2Cu+2H2SO4+O2 ![]() 2CuSO4+2H2O,B项正确;C.加入适量锌粉,发生反应为Zn+Cu2+=Cu+Zn2+,C项正确;D.过滤后直接将溶液蒸发结晶得硫酸锌和硫酸钠的混合物,高温灼烧时,硫酸钠稳定性好,在高温时不分解,硫酸锌在高温时可以分解为氧化锌,但同时产生硫的氧化物污染环境,D项错误,正确的做法是调节溶液的pH,生成Zn(OH)2沉淀,过滤、洗涤后再进行高温灼烧;所以答案选D项。
2CuSO4+2H2O,B项正确;C.加入适量锌粉,发生反应为Zn+Cu2+=Cu+Zn2+,C项正确;D.过滤后直接将溶液蒸发结晶得硫酸锌和硫酸钠的混合物,高温灼烧时,硫酸钠稳定性好,在高温时不分解,硫酸锌在高温时可以分解为氧化锌,但同时产生硫的氧化物污染环境,D项错误,正确的做法是调节溶液的pH,生成Zn(OH)2沉淀,过滤、洗涤后再进行高温灼烧;所以答案选D项。

练习册系列答案
相关题目