题目内容
17.能说明醋酸是弱电解质的事实是( )①用浓硫酸和醋酸钠固体共热可以制得醋酸,②醋酸钠水溶液呈碱性,
③可以用食醋清除水壶中的水垢,④pH=2的醋酸溶液稀释1000倍后的pH<5.
| A. | ①③④ | B. | ①② | C. | ②④ | D. | ② |
分析 强弱电解质的本质区别是电解质的电离程度,部分电离的电解质是弱电解质,只要能说明醋酸部分电离就能证明醋酸是弱电解质,可以根据其强碱盐的酸碱性、根据相同物质的量浓度的溶液导电性强弱、根据一定物质的量浓度的醋酸溶液的pH大小判断等,据此分析解答.
解答 解:①用浓硫酸和醋酸钠固体共热可以制得醋酸,说明醋酸是低沸点的酸,不能说明醋酸部分电离,所以不能证明醋酸是弱电解质,故错误;
②醋酸钠水溶液呈碱性,说明醋酸钠是强碱弱酸盐,则证明醋酸是弱酸,故正确;
③可以用食醋清除水壶中的水垢,说明醋酸酸性大于碳酸,但不能说明醋酸部分电离,所以不能证明醋酸是弱电解质,故错误;
④pH=2的醋酸溶液稀释1000倍后的pH<5,说明醋酸中存在电离平衡,则证明醋酸部分电离,为弱电解质,故正确;
故选C.
点评 本题考查强弱电解质的判断,为高频考点,明确强弱电解质的根本区别是解本题关键,注意不能关键电解质的溶解性强弱判断,为易错点.

练习册系列答案
相关题目
8.利用铜萃取剂M,通过如下反应实现铜离子的富集:

(1)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
(2)基态Cu2+的外围电子排布式为3d9,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律.判断Sc3+、Zn2+的水合离子为无色的依据是3d轨道上没有未成对电子(3d轨道上电子为全空或全满).

(1)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
(2)基态Cu2+的外围电子排布式为3d9,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律.判断Sc3+、Zn2+的水合离子为无色的依据是3d轨道上没有未成对电子(3d轨道上电子为全空或全满).
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
5.在防止禽流感疫情时,防疫部门大量使用了含氯类消毒剂,其中氯胺是一种长效缓释的有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4-5倍,下列有关氯胺(NH2Cl)的说法中一定不正确的是( )
| A. | 氯胺水解产物最初为羟胺(NH2OH)和HCl | |
| B. | 氯胺在一定条件下可与乙烯加成得H2NCH2CH2Cl | |
| C. | 氯胺的消毒原理与漂白粉相似 | |
| D. | 氯胺的电子式为 |
2.某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480mL含NaClO 25%,密度为1.19g/cm3的消毒液.下列说法正确的是( )
| A. | 配制过程只需要三种仪器即可完成 | |
| B. | 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 需要称量的NaClO固体的质量为140 g |
6.已知反应:X+Y=M+N 为放热反应,对该反应的下列说法中正确的是( )
| A. | X 的能量一定高于 M | |
| B. | X 和 Y 的总能量一定高于 M 和 N 的总能量 | |
| C. | Y 的能量一定高于 N | |
| D. | 因为该反应是放热反应,故不必加热反应就一定能发生 |
7.某卤代烃C5H11Cl发生消去反应时,可以得到两种烯烃,则该卤代烃的结构简式可能为( )
| A. | CH3-CH2-CH2-CH2-CH2Cl | B. | 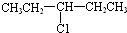 | ||
| C. | 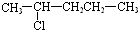 | D. | 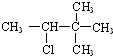 |