题目内容
【题目】传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高。DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量溶液的pH等,所以在中和滴定的研究中应用越来越广泛。
(1)某学习小组利用DIS系统测定某醋酸溶液的物质的量浓度,以测量溶液导电能力来判断滴定终点,实验步骤如下:
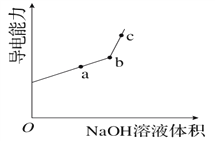
①用__________(填仪器名称)量取20.00 mL醋酸溶液样品,倒入洁净干燥锥形瓶中,连接好DIS系统。如果锥形瓶中含有少量蒸馏水,测量结果将______________(选填“偏大”、“偏小”或“不影响”)。向锥形瓶中滴加0.1000 mol·L-1的NaOH溶液,计算机屏幕上显示出溶液导电能力与加入NaOH溶液体积关系的曲线图如下图。
②醋酸与NaOH溶液反应的离子方程式为___________________________。
③图中b点时,溶液中各离子浓度大小的关系是_________________。
④若图中某一点pH等于8,则c(Na+)—c(CH3COO-)的精确值为________。
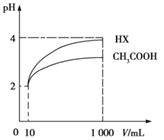
(2)将体积为10 mL pH=2的醋酸溶液与HX溶液分别加水稀释至1 000 mL,稀释过程pH的变化曲线如图所示,则HX的电离平衡常数________(填“大于”“等于”或“小于”,下同)醋酸的电离平衡常数;稀释后,HX溶液中由水电离出来的c(H+)______醋酸溶液中由水电离出来的 c(H+)。
(3)25 ℃时,CH3COOH的电离平衡常数K=1.8×10-5。在0.5 mol·L-1的CH3COOH溶液中由CH3COOH电离出的c(H+)约是由水电离出的c(H+)的______倍。
【答案】 酸式滴定管 不影响 CH3COOH+OH-===CH3COO-+H2O c(Na+)>c(CH3COO-)>c(OH-)>c(H+) 9.9×10-7mol·L-1 大于 大于 3.6×109
【解析】(1)①用酸式滴定管量取20.00mL醋酸溶液样品;锥形瓶中含有少蒸馏水,待测液的物质的量不变,V(标准)不变,根据c(待测)= 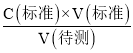 ,c(待测)不变,测量结果将不影响;②醋酸与NaOH溶液反应的离子方程式为:CH3COOH+OH-=CH3COO-+H2O;③图中b点,说明醋酸和NaOH恰好完全反应,醋酸钠水解,使得c(Na+)>c(CH3COO-),故答案为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);④c(H+)=10 -8mol/L,c(OH-)= 10 -6 mol/L,根据电荷守恒c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-),c(Na+)- c(CH3COO-)= c(OH-) - c(H+)=10 -6 mol/L-10 -8mol/L=9.9×10 -7mol/L;(2)由图可知,稀释相同的倍数,HX的pH变化程度大,则酸性HX强,HX的电离平衡常数大于醋酸的电离平衡常数;稀释后,HX电离生成的c(H+)小,对水的电离抑制能力小,所以HX溶液中水电离出来的c(H+)大于醋酸溶液中由水电离出来的 c(H+);(3)25 ℃时,CH3COOH的电离平衡常数K=1.8×10-5。在0.5 mol·L-1的CH3COOH溶液中由CH3COOH电离出的c(H+)约为
,c(待测)不变,测量结果将不影响;②醋酸与NaOH溶液反应的离子方程式为:CH3COOH+OH-=CH3COO-+H2O;③图中b点,说明醋酸和NaOH恰好完全反应,醋酸钠水解,使得c(Na+)>c(CH3COO-),故答案为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);④c(H+)=10 -8mol/L,c(OH-)= 10 -6 mol/L,根据电荷守恒c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-),c(Na+)- c(CH3COO-)= c(OH-) - c(H+)=10 -6 mol/L-10 -8mol/L=9.9×10 -7mol/L;(2)由图可知,稀释相同的倍数,HX的pH变化程度大,则酸性HX强,HX的电离平衡常数大于醋酸的电离平衡常数;稀释后,HX电离生成的c(H+)小,对水的电离抑制能力小,所以HX溶液中水电离出来的c(H+)大于醋酸溶液中由水电离出来的 c(H+);(3)25 ℃时,CH3COOH的电离平衡常数K=1.8×10-5。在0.5 mol·L-1的CH3COOH溶液中由CH3COOH电离出的c(H+)约为![]() ,酸抑制水的电离,则由水电离出的c(H+)= c(OH-)=
,酸抑制水的电离,则由水电离出的c(H+)= c(OH-)= 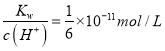 ,由CH3COOH电离出的c(H+)约是由水电离出的c(H+)的
,由CH3COOH电离出的c(H+)约是由水电离出的c(H+)的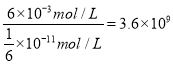 倍。
倍。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案