题目内容
4.根据化学反应的实质是旧键断裂新键形成这一事实,下列变化不属于化学反应的是( )| A. | 白磷在260℃时转化为红磷 | B. | 石墨在高温下转化为金刚石 | ||
| C. | NaCl熔化 | D. | 氧化钙吸水 |
分析 既有旧化学键断裂,又有新化学键形成,说明物质间发生了化学反应,以此分析.
解答 解:A.白磷在260℃时转化为红磷,既有旧化学键断裂,又有新化学键形成,故A错误;
B.石墨在高温下转化为金刚石,既有旧化学键断裂,又有新化学键形成,故B错误;
C.NaCl熔化属于物理过程,只存在旧键的断裂,没有新键生成,故C正确;
D.氧化钙吸水生成氢氧化钙,既有旧化学键断裂,又有新化学键形成,故D错误.
故选C.
点评 本题考查化学键知识,题目难度不大,注意化学变化既有旧化学键断裂,又有新化学键形成.

练习册系列答案
相关题目
14.已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z的二价阳离子与氖原子具有相同的核外电子排布,W与Y同主族,下列说法正确的是( )
| A. | R的原子半径在五种原子中最大 | |
| B. | Y的氢化物的稳定性比W的强 | |
| C. | X与Y形成的化合物只有一种 | |
| D. | R的最高价氧化物的水化物的酸性比W的弱 |
19.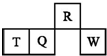 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | T的最高价氧化物对应的水化物不能和强碱反应 |
9.现有部分短周期元素的性质或原子结构如下表:
(1)A的气态氢化物的化学式是H2S,元素B(含8个中子)的一种同位素可测定文物年代,这种同位素的符号是146C.
(2)写出元素F的离子结构示意图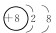 .
.
(3)写出G元素最高价氧化物对应的水化物的化学式是Al(OH)3.
(4)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与氢氧化钠溶液反应
(5)A、B、C、D四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种酸的是H2CO3,理由是碳酸属于弱酸,其它三种酸均为强酸.
(6)C、E、F、G四种元素的单质中化学性质明显不同于其他三种单质的是Al,理由Al具有金属性或是金属.
(7)F的阴离子和G的阳离子的半径大小比较:F->Al3+(用离子符号表示)
(8)A、D的简单离子的还原性强弱:S2->Cl-(用离子符号表示)
| 元素编号 | 元素性质或原子结构 |
| A | 室温下其单质呈粉末状黄色固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| B | 最外层电子数是次外层电子数的2倍 |
| C | 最外层电子数比次外层电子数多3个 |
| D | 元素最高正价是+7价 |
| E | 主族元素中得电子能力最强 |
| F | 空气的主要成分之一,其某种同素异形体是保护地球地表环境的重要屏障 |
| G | 第3周期元素的简单离子中半径最小 |
(2)写出元素F的离子结构示意图
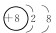 .
.(3)写出G元素最高价氧化物对应的水化物的化学式是Al(OH)3.
(4)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b.
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与氢氧化钠溶液反应
(5)A、B、C、D四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种酸的是H2CO3,理由是碳酸属于弱酸,其它三种酸均为强酸.
(6)C、E、F、G四种元素的单质中化学性质明显不同于其他三种单质的是Al,理由Al具有金属性或是金属.
(7)F的阴离子和G的阳离子的半径大小比较:F->Al3+(用离子符号表示)
(8)A、D的简单离子的还原性强弱:S2->Cl-(用离子符号表示)
16.下列离子方程式书写不正确的是( )
| A. | 单质铜与稀硝酸反应:Cu+2 H++2NO3-═Cu2++2 NO↑+H2O | |
| B. | NaOH溶液与足量的Ca(HCO3)2溶液反应:2HCO3-+2OH-+Ca2+═CaCO3↓+2H2O | |
| C. | 等物质的量的FeBr2和Cl2在溶液中的反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 氨水吸收少量的二氧化硫:2NH3•H2O+SO2═2NH4++SO32-+H2O |
13.常温下,下列各溶液中,酸性最强的是( )
| A. | pH=3 | B. | c(H+)=5×10-5mol/L | ||
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=6 | D. | c(OH-)=10-12mol/L的溶液 |
14.如表是不同温度下水的离子积数据:
若25<t1<t2,则α>(填“<”“>”或“=”)1×10-14.
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-12 |
 .
.