题目内容
(18分)工业上以黄铜矿(主要成分CuFeS2)为原料制备CuSO2·5H2O的主要流程如下:
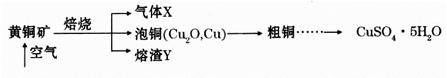
(1)下列装置可用于吸收气体X的是___________(填代号)。
(2)某研究性学习小组用泡铜与CO反应来制取粗铜。
①装置B中的药品为_____________。
②实验时,依次进行如下操作:组装仪器、__________________、加装药品、通入气体、_____________________、点燃酒精灯。


(3)熔渣Y的成分为Fe2O3和FeO,选用提供的试剂,设计实验验证熔渣中含有FeO。写出有关实验操作、现象与结论。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、氯水。
_______________________________________________________________________。
(4)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中H2SO4与HNO3的最佳物质的量之比为___________________。
(5)用滴定法测定所得产品中CuSO4·5H2O的含量,称取a g样品配成100 mL溶液,取出20.00 mL,用c mol·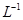 滴定剂EDTA(H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂b mL。滴定反应如下:
滴定剂EDTA(H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂b mL。滴定反应如下: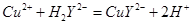 。则CuSO4·5H2O质量分数为__________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏_______。
。则CuSO4·5H2O质量分数为__________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏_______。

(1)下列装置可用于吸收气体X的是___________(填代号)。
(2)某研究性学习小组用泡铜与CO反应来制取粗铜。
①装置B中的药品为_____________。
②实验时,依次进行如下操作:组装仪器、__________________、加装药品、通入气体、_____________________、点燃酒精灯。


(3)熔渣Y的成分为Fe2O3和FeO,选用提供的试剂,设计实验验证熔渣中含有FeO。写出有关实验操作、现象与结论。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、氯水。
_______________________________________________________________________。
(4)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中H2SO4与HNO3的最佳物质的量之比为___________________。
(5)用滴定法测定所得产品中CuSO4·5H2O的含量,称取a g样品配成100 mL溶液,取出20.00 mL,用c mol·
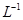 滴定剂EDTA(H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂b mL。滴定反应如下:
滴定剂EDTA(H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂b mL。滴定反应如下: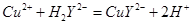 。则CuSO4·5H2O质量分数为__________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏_______。
。则CuSO4·5H2O质量分数为__________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏_______。(1)bd
(2)①碱石灰②检查装置气密性;收集CO检验纯度
(3)取少量熔渣,加过量稀硫酸溶解,然后向滤液中加少量KMnO4溶液,若溶液紫色退去,则说明熔渣中含有FeO
(4)3:2
(5) ;高
;高
(2)①碱石灰②检查装置气密性;收集CO检验纯度
(3)取少量熔渣,加过量稀硫酸溶解,然后向滤液中加少量KMnO4溶液,若溶液紫色退去,则说明熔渣中含有FeO
(4)3:2
(5)
 ;高
;高试题分析:(1)气体X是SO2,可用NaOH溶液吸收,注意防止倒吸,故可选用bd;(2)①用泡铜制取粗铜是利用CO与Cu2O反应来得到Cu,同时生成CO2,故装置B干燥管内应放碱石灰;②实验时,依次进行的操作为:组装仪器、检查装置气密性、加装药品、通入气体、收集CO检验纯度、点燃酒精灯;(3)验证熔渣中含有FeO,可以利用亚铁离子的还原性,操作为:取少量熔渣,加过量稀硫酸溶解,然后向滤液中加少量KMnO4溶液,若溶液紫色退去,则说明熔渣中含有FeO;(4)铜不与稀硫酸反应,但可溶解在硝酸中,反应的离子方程式为3Cu+8H++2NO=3Cu2++2NO↑+4H2O,由此可知当硝酸与硫酸物质的量之比为2:3时,硝酸全部转化为NO,此时溶液中溶质为CuSO4,即混酸中H2SO4与HNO3的最佳物质的量之比为3:2;(5)根据所给反应可知n(Cu2+)=n(H2Y2-),所以CuSO4·5H2O的质量分数为
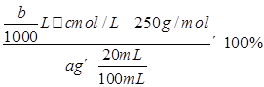 =
=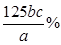 。
。
练习册系列答案
相关题目