题目内容
【题目】一定条件下,在容积恒为2.0L的容器中,Fe和CO2发生如下反应: CO2(g) + Fe(s) ![]() FeO(s) + CO(g),若起始时向容器中加入1mol CO2,5.0 min后,容器内气体的相对平均分子量为32,则这段时间内ν(CO2)=_____________。
FeO(s) + CO(g),若起始时向容器中加入1mol CO2,5.0 min后,容器内气体的相对平均分子量为32,则这段时间内ν(CO2)=_____________。
①下列说法不正确的是_______
a 当混合气体的密度不变时说明反应达到了平衡
b 混合气体的平均相对分子质量不变时说明反应达到了平衡
c 平衡后移除二氧化碳时,正反应速率一直减小直至建立新的平衡
d 平衡后缩小容器的体积,正逆反应速率不变,平衡不移动
②待反应达到平衡后再充入一定量的二氧化碳,平衡向_________移动(选填“正向”、 “逆向”、或“不”),二氧化碳的转化率________(填“增大”,“减小”或“不变”),CO的物质的量____(选填“增大”,“减小”或“不变”)。
【答案】0.075mol/(L·min) c、d 正向 不变 增大
【解析】
若起始时向容器中加入1mol![]() ,
,![]() 后,容器内气体的相对平均分子量为32,三行式解如下:
后,容器内气体的相对平均分子量为32,三行式解如下:
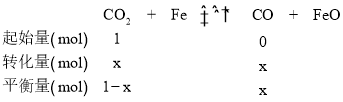
![]() =32,解得x=0.75,所以
=32,解得x=0.75,所以 ;故答案为:
;故答案为:![]() 。
。
①![]() .当混合气体的密度是变量,不变时说明反应达到了平衡,正确;
.当混合气体的密度是变量,不变时说明反应达到了平衡,正确;
![]() 混合气体的平均相对分子质量是变量,不变时说明反应达到了平衡,正确;
混合气体的平均相对分子质量是变量,不变时说明反应达到了平衡,正确;
![]() 平衡后移除二氧化碳时,正反应速率先减小后增大,直至建立新的平衡,故错误;
平衡后移除二氧化碳时,正反应速率先减小后增大,直至建立新的平衡,故错误;
![]() 平衡后缩小容器的体积,正逆反应速率增大,但平衡不移动,故错误。
平衡后缩小容器的体积,正逆反应速率增大,但平衡不移动,故错误。
故答案为:cd。
②待反应达到平衡后再充入一定量的二氧化碳,平衡向正向移动,但到达新平衡时的效果与原平衡等效,故二氧化碳的转化率不变,CO的物质的量增大,故答案为:正向;不变;增大。

练习册系列答案
相关题目