题目内容
下列实验不能达到预期目的是( )
| A、用饱和NaHCO3溶液除去CO2中少量的HCl |
| B、用醋和澄清石灰水验证蛋壳中含有碳酸盐 |
| C、在试管中煮沸液体时,加碎石片可防止暴沸 |
| D、用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42- |
考点:化学实验方案的评价,化学实验安全及事故处理,物质的分离、提纯和除杂,常见阴离子的检验,物质的检验和鉴别的基本方法选择及应用
专题:实验评价题
分析:A.NaHCO3可与HCl反应生成CO2;
B.醋酸与碳酸盐反应生成二氧化碳,二氧化碳可使澄清石灰水变浑浊;
C.碎石可防止液体暴沸;
D.可能生成AgCl沉淀.
B.醋酸与碳酸盐反应生成二氧化碳,二氧化碳可使澄清石灰水变浑浊;
C.碎石可防止液体暴沸;
D.可能生成AgCl沉淀.
解答:
解:A.NaHCO3可与HCl反应生成CO2,可用于除杂,故A正确;
B.醋酸与碳酸盐反应生成二氧化碳,二氧化碳可使澄清石灰水变浑浊,可用于检验,故B正确;
C.碎石可防止液体暴沸,故C正确;
D.不能排除Ag+或SO32-离子的影响,可先加盐酸,如无现象,再加氯化钡检验,如生成沉淀,可证明含有SO42-,故D错误.
故选D.
B.醋酸与碳酸盐反应生成二氧化碳,二氧化碳可使澄清石灰水变浑浊,可用于检验,故B正确;
C.碎石可防止液体暴沸,故C正确;
D.不能排除Ag+或SO32-离子的影响,可先加盐酸,如无现象,再加氯化钡检验,如生成沉淀,可证明含有SO42-,故D错误.
故选D.
点评:本题考查较为综合,涉及物质的除杂、检验等知识,为高考常见题型,侧重于学生的分析能力能力和实验能力的考查,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列离子方程式中不正确的是( )
| A、过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| C、氢氧化钠和少量氢硫酸反应:2OH-+H2S=S2-+2H2O |
| D、在澄清石灰水中通入过量二氧化碳:OH-+CO2=HCO3- |
下列判断错误的是( )
| A、沸点:NH3>AsH3>PH3 |
| B、熔点:SiO2>CO2>CS2 |
| C、酸性:H2SO4>H3PO4>H2CO3 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
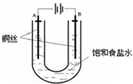 已知:Kap(CuCl,白色)=1.2×10-6,Kap(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-=CuCl.下列说法不正确的是( )
已知:Kap(CuCl,白色)=1.2×10-6,Kap(CuOH,橙黄色)=1.2×10-14.如图,用铜电极电解饱和食盐水时,阳极发生的电极反应为Cu-e-+Cl-=CuCl.下列说法不正确的是( )| A、B极发生的电极反应为2H++2e-=H2↑ |
| B、实验开始时,A极附近出现白色浑浊 |
| C、电解时,Na+移向A极 |
| D、一段时间后,U形管底部形成橙黄色沉淀 |
在下列溶液中,各组离子可能大量共存的是( )
| A、pH>7的溶液中:Na+、Cl-、Ba2、Fe3+ |
| B、有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- |
| C、由水电离的c(H+)=10-13mol?L-1的溶液中:Al3+、K+、NO3-、SO42- |
| D、碳酸氢钠溶液中:K+、ClO-、Cl-、OH- |
25℃时,pH值都等于11的NaOH溶液和Na2CO3溶液中,由水电离出的OH-浓度( )
| A、相等,均为10-3mol?L-1 |
| B、相等,均为10-11mol?L-1 |
| C、NaOH溶液中为10-3mol?L-1 |
| D、Na2CO3溶液中为10-3mol?L-1 |
下列说法不正确的是( )
| A、胶状沉淀或颗粒太小的沉淀不宜用减压过滤,溶液有强酸性、强碱性或强氧化性时,应用玻璃纤维代替滤纸或用玻璃砂漏斗代替布氏漏斗 |
| B、移液管吸取溶液后,应将其垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
| C、红外光谱仪、质谱仪、核磁共振仪可用于测定有机物结构,同位素示踪法可用于研究化学反应历程 |
| D、为检验火柴头中是否存在氯元素,将火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸溶液.若出现白色沉淀,说明含氯元素 |
实现下列变化,必须要加入还原剂的是( )
| A、Cl2→HClO |
| B、Fe→FeCl3 |
| C、NaI→AgI |
| D、MnO4-→Mn2+ |