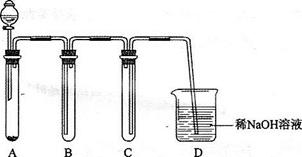
题目内容
下列制备物质的设计中,理论上正确、操作上可行、经济上合理的是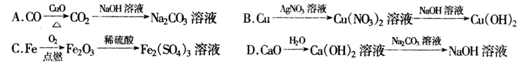
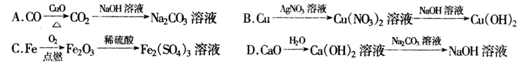
D
A选项中的第一步操作较难控制,C的利用率低,且生成的CO污染大气,不可选;B选项中的AgNO3是一种比较昂贵的药品,该制备流程经济效益差;C项中Fe点燃生成的是Fe3O4,得不到纯净的Fe2(SO4)3溶液。Ca(OH)2微溶,溶解的Ca(OH)2都变成CaCO3沉淀了,于是,更多的Ca(OH)2溶解,接着沉淀,然后又溶,。。。最后,所有的Ca(OH)2都溶解了,当然也就都变成当然也就只有NaOH了,故D可以。

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案
相关题目

 等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下: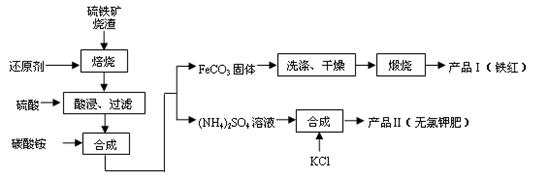
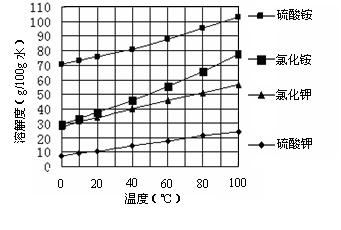
 液。判断Ba(NO3)2已过量的方法是 。
液。判断Ba(NO3)2已过量的方法是 。
 器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。
器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。 会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。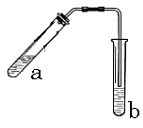
 出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)
出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)

 mL D.200mL
mL D.200mL ▲ 。
▲ 。 水至刻度处
水至刻度处 1)下图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
1)下图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。