题目内容
20.难溶于水而且比水轻的含氧有机物是( )①植物油
②乙酸
③乙酸乙酯.
| A. | ①②③ | B. | ①② | C. | ①③ | D. | ②③ |
分析 植物油、乙酸乙酯、乙酸密度都比水小,而植物油和乙酸乙酯均不溶于水,而乙酸能溶于水,据此分析.
解答 解:①植物油不溶于水且密度比水小,且植物油属于酯类,故为含氧的有机物,故正确;
②乙酸属于羧酸类,为含氧有机物,但乙酸溶于水,故错误;
③乙酸乙酯不溶于水且密度比水小,且乙酸乙酯属于酯类,故为含氧的有机物,故正确;
故选C.
点评 本题考查有机物的物理性质和元素组成,难度不大,联系生活实际来理解有机物的物理性质.

练习册系列答案
相关题目
6.新型镁铝合金(Mg17Al12)有储氢性能,它一定条件下完全吸氢的反应为:Mg17Al12+17H2═17MgH2+12Al,得到的混合物Y(17MgH2+12Al)能与酸反应释放出大量氢气.下列说法正确的是( )
| A. | 该合金应在氮气保护下,将一定比例的Mg、Al单质熔炼而成 | |
| B. | 该合金中含有离子键,铝元素呈正价 | |
| C. | 1mol Mg17Al12完全吸氢后得到的Y与盐酸完全反应放出H2在标准状况下的体积为1164.8L | |
| D. | 合金的熔点高于金属镁、金属铝的熔点 |
8.下列实验装置或对实验的描述正确的是( )
| A. |  稀释浓硫酸 | B. | 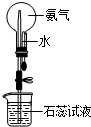 红色喷泉 | C. |  检验乙烯 | D. | 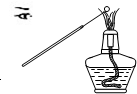 观察钾离子焰色 观察钾离子焰色 |
15.几种短周期元素的原子半径及主要化合价如表:
下列叙述正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径/pm | 186 | 143 | 75 | 71 |
| 主要化合价 | +1 | +3 | +5、+3、-3 | -1 |
| A. | X、Y元素的金属性X<Y | |
| B. | Z的气态氢化物比W的气态氢化物稳定 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 四种元素对应的简单离子的离子半径大小顺序为Z3->W->X+>Y3+ |
5.下列图示实验操作正确的是( )
| A. |  除去CL2中的HCL | B. |  电解制CL2和H2 | C. | 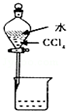 分离CCL4和水 | D. |  中和热的测定 |
12.根据原子结构及元素周期律的知识,下列推断正确的是( )
| A. | 基态原子的4S能级中只有1个电子的元素共有4种 | |
| B. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力不相同 | |
| C. | Cl-、S2-、Na+、K+半径逐渐减小 | |
| D. | 最外层有3个未成对电子的原子一定属于主族元素 |
9.下列有关物质的描述及其应用均正确的是( )
| A. | 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 | |
| B. | FeCl3具有氧化性,用FeCl3溶液刻蚀印刷电路板 | |
| C. | Na2O2中含有O2,所以用过氧化钠可为潜水艇舱提供氧气 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
10.已知:H2S在与不足量的O2反应时,生成S和H2O.根据以下三个热化学方程式:
2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1
2H2S(g)+O2(g)═2S(s)+2H2O(l)△H2
2H2S(g)+O2(g)═2S(s)+2H2O(g)△H3
判断△H1、△H2、△H3三者大小关系正确的是( )
2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1
2H2S(g)+O2(g)═2S(s)+2H2O(l)△H2
2H2S(g)+O2(g)═2S(s)+2H2O(g)△H3
判断△H1、△H2、△H3三者大小关系正确的是( )
| A. | △H3>△H2>△H1 | B. | △H1>△H3>△H2 | C. | △H1>△H2>△H3 | D. | △H2>△H1>△H3 |