��Ŀ����
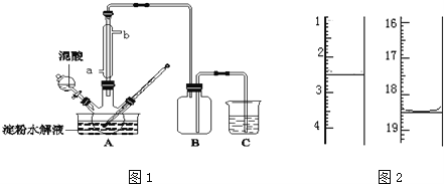
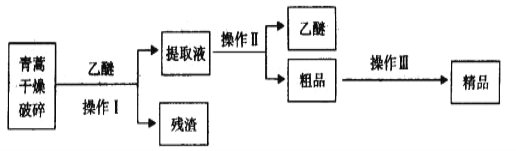
����Ŀ������������ȡ�����صķ���֮һ������ȡԭ��Ϊ�����ġ����ѽ�ȡ������Ҫ������ͼ��ʾ��
��֪�������������ĺ��������Ϊ��ɫ��״���壬�����ڱ�ͪ���ȷºͱ��У��ڼ״����Ҵ������ѡ�ʯ�����п��ܽ⣬��ˮ�м������ܣ��۵�Ϊ156-157�棬���ȶ��Բ�������Ǹ�Ч�Ŀ�űҩ�����ѷе�Ϊ35�档��������������ǣ� ��
A.�������������������ѵ�Ŀ�����ܽ�������
B.��������Ҫ�IJ���������Ҫ���ձ���©����������
C.������������ǹ���
D.���������Ҫ���̿����Ǽ�95%���Ҵ���Ũ�����ᾧ������
���𰸡�C
��������
��������ﵷ�飬�������ܽ������أ����˳�ȥ�����õ���ȡҺ������ȡҺ����õ������ش�Ʒ���ٽ���Ʒ��95%���Ҵ��ܽ⡢Ũ�����ᾧ�����˵õ���Ʒ��
A���������������������ѵ�Ŀ���ǽ������ش��������ܽ������A��ȷ��
B���������ǹ��˲�������Ҫ�IJ���������Ҫ���ձ���©������������B��ȷ��
C��������������C����
D�����������Ҫ�����Ǽ�95%���Ҵ��ܽ⣬Ũ�����ᾧ�����˵õ���Ʒ��D��ȷ��
��ѡC��

����Ŀ���ⶨ����ͭ���壨CuSO4XH2O ����Xֵ��ʵ��������£�
![]()
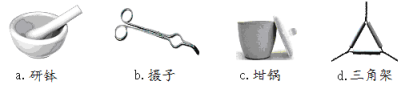
��1��������ʵ�����õ��ļ����������������Ӧ������ȷ����___________��
��2�������ա�ʱ��Դѡ�õ��Ǿƾ��ƶ����Ǿƾ���ƣ�������_____________________������ȴ������_______________��(����������)��
��3�� �����ء�������Ŀ����_________________________________________________��
�жϡ����ء���������_________________________________________________��
��4��������ijѧ��ʵ���һ�����ݣ�����ɼ���
�������� | �����뾧�������� | ���Ⱥ���������������� |
11.721g | 22.692g | 18.631g |
X=__________________��(��ȷ��0.01)��ʵ����������_________________��(����С�����һλ)
��5�����ʵ���в�������ԭ�������__________����ɵġ�
a������ͭ�����к��в��ӷ������ʡ��� b���ڼ��ȹ��̷����к�ɫ��������
c������ʱ�о���ɽ����������������� d������ʧˮ��¶���ڿ�������ȴ
����Ŀ������ͭ�����ᷴӦ������ͭ��
(1)��������ᾧˮ�����ⶨʵ���У����ز�����ɵı���______________��
(2)������ͼװ�ü�����ˮ����ͭ��ĩֱ����ȫ�ֽ⣬A���Թ���ʣ���ɫ��ĩ���ô����ǵ�ľ�����뼯��ƿD������ľ���ܸ�ȼ����Ӧǰ���װ�õ�������ͼ�·��ı�����ʾ��

װ�� | A(�Թ�+��ĩ) | B | C |
��Ӧǰ | 50.0 g | 70.0 g | 540.0 g |
��Ӧ�� | 45.0 g | 74.5 g | 540.0 g |
��ͨ�����㣬�ƶϸ�ʵ������������ͭ�ֽ�Ļ�ѧ����ʽ��_______________��