题目内容
【题目】根据下表给出的几种物质的熔点、沸点数据判断说法中错误的是 ( )

A. SiCl4是分子晶体 B. MgCl2中键的强度比NaCl中键的强度小
C. 单质R是原子晶体 D. AlCl3为离子晶体
【答案】D
【解析】试题分析:根据表格中氯化物的熔沸点判断物质的晶体类型,一般离子晶体的熔沸点大于分子晶体的熔沸点。
A.由表格中的数据可知SiCl4的熔沸点较低,则SiCl4是分子晶体,故对;
B.由表格中的数据可知,NaCl的熔点高,则MgCl2比NaCl更容易熔化,MgCl2中键的强度比NaCl中键的强度小,故对.
C.由表格中的数据可知,单质B的熔沸点很高,则可能为原子晶体,故对;
D.由表格中的数据可知,AlCl3的熔点比沸点较低,所以在加热时能升华,应为分子晶体,故错;
故选D。

练习册系列答案
相关题目
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并将产生的气体全部通过如图所示装置,得到如下表所列的实验结果(假设产生的气体完全被吸收)。
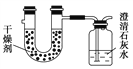
实验前 | 实验后 | |
干燥剂和U形管的质量 | 101.1 g | 102.9 g |
石灰水和广口瓶的质量 | 312.0 g | 314.2 g |
根据实验数据填空:
(1)实验完毕后,生成物中水的质量为________ g,假设广口瓶里生成一种正盐,其质量为________ g。
(2)生成的水中氢元素的质量为________ g。
(3)生成的CO2中碳元素的质量为________ g。
(4)该燃料中碳、氢元素的质量比为________。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为________,结构简式为________。