题目内容
2.2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的.因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2).导电乙炔黑(一种炭黑).铝箔以及有机粘接剂.某回收工艺流程如下: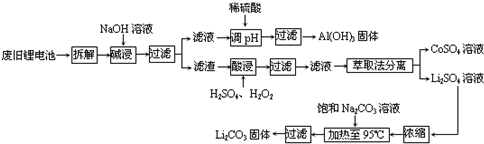
(1)上述工艺回收到的产物有Al(OH)3、CoSO4、Li2CO3.
(2)废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是隔绝空气和水分.
(3)碱浸时主要反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(4)酸浸时反应的化学方程式为2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O.如果用盐酸代替H2SO4和H2O2的混合液也能达到溶解的目的,但不利之处是有氯气生成,污染较大.
(5)生成Li2CO3的化学反应方程式为Li2SO4+Na2CO3=Na2SO4+Li2CO3↓.已知Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应趁热
(6)CO和铁粉在一定条件下可以合成五羰基合铁[Fe(CO)5],该物质可用作无铅汽油的防爆剂,是一种浅黄色液体,易溶于苯等有机溶剂,不溶于水,光照时生成Fe2(CO)9,60℃发生自燃. 今将一定量的Fe(CO)5的苯溶液,用紫外线照射片刻.取照射后的溶液完全燃烧,得到30.58gCO2、5.4gH2O及1.6g红棕色粉末.红棕色粉末的化学式为Fe2O3,照射后的溶液中Fe(CO)5和Fe2 (CO)9的物质的量之比为2:1.
分析 铝钴膜废料中含有LiCo02和铝箔,将废料先用碱液浸泡,将Al充分溶解,过滤后得到的滤液为含有偏铝酸钠,滤渣为LiCo02;通过调节滤液的pH,将偏铝酸钠转化成氢氧化铝沉淀;将滤渣用双氧水、硫酸处理后生成Li2SO4、CoSO4,反应的离子方程式为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O,通过操作分别分离出Li2SO4、CoSO4,通过浓缩、加入饱和碳酸钠溶液后过滤,最后得到碳酸锂固体,
(1)根据工艺流程的最终产物可判断回收到的产物,应为Al(OH)3、CoSO4、Li2CO3;
(2)从金属锂的化学性质分析,锂为活泼金属;
(3)根据所加入的反应物以及生成物结合质量守恒定律和电荷守恒定律来书写离子方程式;
(4)根据所加入的反应物以及生成物结合质量守恒定律来书写化学方程式;由题中信息知LiCoO2具有强氧化性,加入盐酸有污染性气体氯气生成;
(5)根据质量守恒定律来书写化学方程式,Li2CO3在水中的溶解度随着温度的升高而减小,应趁热过滤;
(6)依据含铁的化合物的颜色判断产物;依据铁原子和碳原子个数守恒计算解答Fe(CO)5和Fe2(CO)9的物质的量之比.
解答 解:铝钴膜废料中含有LiCo02和铝箔,将废料先用碱液浸泡,将Al充分溶解,过滤后得到的滤液为含有偏铝酸钠,滤渣为LiCo02;通过调节滤液的pH,将偏铝酸钠转化成氢氧化铝沉淀;将滤渣用双氧水、硫酸处理后生成Li2SO4、CoSO4,反应的离子方程式为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O,通过操作分别分离出Li2SO4、CoSO4,通过浓缩、加入饱和碳酸钠溶液后过滤,最后得到碳酸锂固体,
(1)工艺流程的最终产物为:Al(OH)3、CoSO4、Li2CO3,故答案为:Al(OH)3、CoSO4、Li2CO3;
(2)金属锂性质活泼,易与氧气、水发生反应,应隔绝空气和水分,故答案为:隔绝空气和水分;
(3)铝能与碱反应生成AlO2-,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)酸浸时反应物有硫酸、过氧化氢以及LiCoO2,生成物有Li2SO4和CoSO4,反应方程式为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O,由题中信息知LiCoO2具有强氧化性,加入盐酸有污染性气体氯气生成,
故答案为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O;有氯气生成,污染较大;
(5))碳酸锂难溶,生成Li2CO3的化学反应属于复分解反应,方程式为Li2SO4+Na2CO3=Na2SO4+Li2CO3↓,Li2CO3在水中的溶解度随着温度的升高而减小,应趁热过滤,
故答案为:Li2SO4+Na2CO3=Na2SO4+Li2CO3↓;趁热;
(6)铁的化合物中只有Fe2O3为红棕色,所以该固体为Fe2O3,5.4g H2O为苯燃烧生成,则
C6H6~6CO2~3H2O
6 3
n(CO2) $\frac{5.4g}{18g/mol}$
得 n(CO2)=0.6mol
设Fe(CO)5的物质的量为xmol,Fe2(CO)9的物质的量为ymol,
则依据铁原子个数守恒可知,x+2y=$\frac{1.6g}{160g/mol}$×2=0.02mol;
依据碳原子个数守恒可知:5x+9y=$\frac{30.58g}{44g/mol}$-0.6mol=0.095mol;
解得:x=0.01mol y=0.005mol x:y=2:1;
故答案为:Fe2O3;2:1.
点评 本题为生产流程题,涉及金属的回收、环境保护、氧化还原反应、物质的分离提纯和除杂等问题,考查了实验的设计,方程式的书写,化学平衡表达式的书写,物质的量的计算题目较为综合,做题时注意仔细审题,从题目中获取关键信息.本题难度中等.

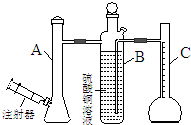
| A. | 反应前后抽气使B中导管内外液面持平 | |
| B. | 用饱和食盐水代替A装置中的蒸馏水 | |
| C. | 把A装置浸入盛有冰水混合物的水槽中 | |
| D. | 在B装置中的硫酸铜溶液表面覆盖一层苯 |
| A. | 用碳酸钠溶液可以洗涤油污 | B. | 用pH试纸可以测定土壤的酸碱性 | ||
| C. | 用明矾可以对自来水杀菌病毒 | D. | 含氟牙膏可以有效防止龋齿 |
| A. | 因为s轨道的形式是球形的,所以处于s轨道上的电子做的是圆周运动 | |
| B. | 电子在3px、3py、3ps三个轨道上运动时,能量不同 | |
| C. | 电子云是用来形象的描述电子运动状态的 | |
| D. | H、F、Cl、O的电负性逐渐增大 |
| A. | 点燃 | B. | 通过溴水 | C. | 催化加氢 | D. | 通过石灰水 |