题目内容
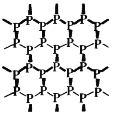
【题目】有一种矿石,经测定含有镁、硅、氧三种元素且它们的质量比为12∶7∶16。
(1)用盐的组成表示其化学式: ___________。
(2)用氧化物的组成表示其化学式: _______。
(3)该矿石的成分属于________(填物质的分类)。
(4)写出该矿石(氧化物形式)与盐酸反应的化学方程式: ______。
【答案】Mg2SiO4 2MgO·SiO2 硅酸盐 2MgO·SiO2+4HCl=2MgCl2+2H2O+SiO2
【解析】
根据n=![]() 及原子个数比=原子的物质的量之比进行计算,得出正确结论;由金属离子和酸根离子组成的化合物属于盐。
及原子个数比=原子的物质的量之比进行计算,得出正确结论;由金属离子和酸根离子组成的化合物属于盐。
镁、硅、氧的质量比为12:7:16,则镁、硅、氧的原子个数比为![]() :
:![]() :
:![]() =2:1:4
=2:1:4
(1)该矿石用盐的组成可表示为:Mg2SiO4;
(2)该矿石用氧化物的组成可表示为:2MgOSiO2
(3)Mg2SiO4属于盐类,且属于硅酸盐;
(4)Mg2SiO4溶于与稀盐酸生成MgCl2和SiO2,发生反应的化学方程式为2MgO·SiO2+4HCl=2MgCl2+2H2O+SiO2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目