题目内容
水杨酸甲酯(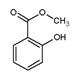 )具有冬青味,故又名冬青油,主要用于制造杀虫剂、杀菌剂、香料、涂料等。用水杨酸(
)具有冬青味,故又名冬青油,主要用于制造杀虫剂、杀菌剂、香料、涂料等。用水杨酸(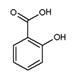 )与甲醇酯化而得的冬青油中往往会混有未反应完全的水杨酸,若要进行提纯,适宜的洗涤剂为( )
)与甲醇酯化而得的冬青油中往往会混有未反应完全的水杨酸,若要进行提纯,适宜的洗涤剂为( )
 )具有冬青味,故又名冬青油,主要用于制造杀虫剂、杀菌剂、香料、涂料等。用水杨酸(
)具有冬青味,故又名冬青油,主要用于制造杀虫剂、杀菌剂、香料、涂料等。用水杨酸( )与甲醇酯化而得的冬青油中往往会混有未反应完全的水杨酸,若要进行提纯,适宜的洗涤剂为( )
)与甲醇酯化而得的冬青油中往往会混有未反应完全的水杨酸,若要进行提纯,适宜的洗涤剂为( )| A.NaHCO3溶液 | B.NaOH溶液 | C.Na2CO3溶液 | D.NaCl溶液 |
A
试题分析:因NaHCO3溶液与苯酚不反应,所以不与水杨酸甲酯中酚羟基反应,但水杨酸有羧基可以和NaHCO3溶液反应,从而起到除杂的作用。而NaOH和Na2CO3溶液 与水杨酸甲酯反应,不能用来除杂。选A。

练习册系列答案
相关题目
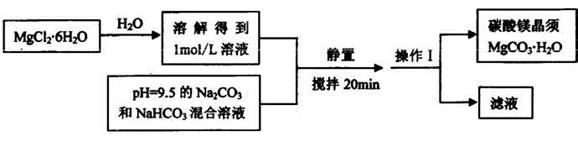
 Fe2+ + Ag+。下列铁盐中洗涤效果最好的是
Fe2+ + Ag+。下列铁盐中洗涤效果最好的是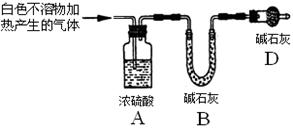
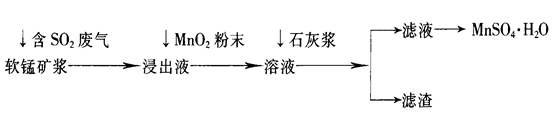
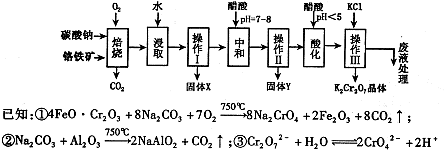

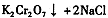 。该反应在溶液中能发生的理由是: 。
。该反应在溶液中能发生的理由是: 。