��Ŀ����
������ʾ��þ�뱥��̼��������Һ��Ӧ������������Ͱ�ɫ�����ijͬѧ���������ʵ�鷽������֤���̽����Ӧԭ����
��1���������
ʵ��I����ɰֽ��ȥþ����������Ĥ���������ʢ���������з�̪�ı���̼��������Һ���Թ��У�Ѹ�ٷ�Ӧ�������������ݺͰ�ɫ�������Һ��dz���졣
��ͬѧ�Է�Ӧ�в����İ�ɫ�������������²²⣺
�²�1����ɫ���������Ϊ ��
�²�2����ɫ���������ΪMgCO3��
�²�3����ɫ����������Ǽ�ʽ̼��þ[xMgCO3��yMg(OH)2]��
��2����ƶ���ʵ��ȷ�����ﲢ��֤�²⣺
��3��Ϊ��һ��ȷ��ʵ��I�IJ����ƶ���ʵ�鷽������ͼ��ʾ��
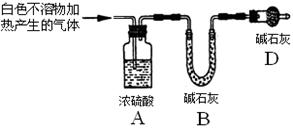
��ȡʵ��������ø�������İ�ɫ������22.6 g����ּ��������ٲ�������Ϊֹ����ʹ�ֽ����������ȫ������װ��A��B�С�ʵ��ǰ��װ��A����1.8 g��װ��B����8.8 g����ȷ����ɫ������Ļ�ѧʽ ��
��4�����ϻ�ѧ����ͻ�ѧƽ���ƶ�ԭ������Mg��NaHCO3��Һ��Ӧ�����������ݵ�ԭ��_________��
��1���������
ʵ��I����ɰֽ��ȥþ����������Ĥ���������ʢ���������з�̪�ı���̼��������Һ���Թ��У�Ѹ�ٷ�Ӧ�������������ݺͰ�ɫ�������Һ��dz���졣
��ͬѧ�Է�Ӧ�в����İ�ɫ�������������²²⣺
�²�1����ɫ���������Ϊ ��
�²�2����ɫ���������ΪMgCO3��
�²�3����ɫ����������Ǽ�ʽ̼��þ[xMgCO3��yMg(OH)2]��
��2����ƶ���ʵ��ȷ�����ﲢ��֤�²⣺
| ʵ����� | ʵ�� | ʵ������ | ���� |
| ʵ��� | ��ʵ��I���ռ����������ȼ | �ܰ���ȼ�ա���������ɫ���� | ����ɷ�Ϊ___?___ |
| ʵ��� | ȡʵ��I�еİ�ɫ�����ϴ�ӣ��������� ? | ? | ��ɫ��������ܺ���MgCO3 |
| ʵ��� | ȡʵ��I�еij���Һ�������м�������CaCl2ϡ��Һ | ������ɫ���� | ��Һ�д��� �� ���� |

��ȡʵ��������ø�������İ�ɫ������22.6 g����ּ��������ٲ�������Ϊֹ����ʹ�ֽ����������ȫ������װ��A��B�С�ʵ��ǰ��װ��A����1.8 g��װ��B����8.8 g����ȷ����ɫ������Ļ�ѧʽ ��
��4�����ϻ�ѧ����ͻ�ѧƽ���ƶ�ԭ������Mg��NaHCO3��Һ��Ӧ�����������ݵ�ԭ��_________��
����9�֣�
��1���²�1��Mg(OH)2��1�֣�
��2�������� ����ϡ���ᣨ�������ɣ���
�۲������ݣ�����ȫ���ܽ� ����CO2- 3����1�֣�
��3�� 2MgCO3��Mg(OH)2 �� Mg(OH)2��2MgCO3 �� Mg3(OH)2(CO3)2
��4��NaHCO3��Һ�д�������ƽ�⣺HCO- 3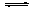 H+ +CO2- 3��H2O
H+ +CO2- 3��H2O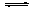 H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
��1���²�1��Mg(OH)2��1�֣�
��2�������� ����ϡ���ᣨ�������ɣ���
�۲������ݣ�����ȫ���ܽ� ����CO2- 3����1�֣�
��3�� 2MgCO3��Mg(OH)2 �� Mg(OH)2��2MgCO3 �� Mg3(OH)2(CO3)2
��4��NaHCO3��Һ�д�������ƽ�⣺HCO- 3
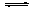 H+ +CO2- 3��H2O
H+ +CO2- 3��H2O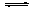 H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2�����������
��1�������֪�²�ΪMg(OH)2
��2����þ��ˮ��Ӧ�����������ڼ��̼����һ��������ᡣ�ۿ��Ƿ��ж�����̼���ɡ�����Һ����CO32-��Ca2+���ɰ�ɫ������
��3����������ɵù�ϵʽMg(OH)2~H2O��MgCO3~CO2��n(H2O)=1.8g/18g/mol=0.1mol��n(CO2)=8.8g/44g/mol=0.2mol����֪Ϊ2MgCO3��Mg(OH)2 �� Mg(OH)2��2MgCO3 ��Mg3(OH)2(CO3)2 ��
��4��NaHCO3��Һ�д�������ƽ�⣺HCO- 3
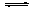 H+ +CO2- 3��H2O
H+ +CO2- 3��H2O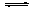 H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
H++OH-��Mg��H+��Ӧ����H2��Mg2+��Mg2+��OH-��CO32-����������Mg(OH)2��2MgCO3����H+��OH-��CO2- 3��Ũ�Ⱦ����ͣ���ʹ������ƽ��������ƶ�����Mg�ͱ���NaHCO3��Һ��Ӧ������������H2��
��ϰ��ϵ�д�
�����Ŀ

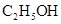 ��Ũ����170�湲�ȣ��Ƶõ�����ͨ������
��Ũ����170�湲�ȣ��Ƶõ�����ͨ������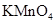 ��Һ
��Һ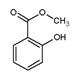 �����ж���ζ�������������ͣ���Ҫ��������ɱ�����ɱ���������ϡ�Ϳ�ϵȡ���ˮ���ᣨ
�����ж���ζ�������������ͣ���Ҫ��������ɱ�����ɱ���������ϡ�Ϳ�ϵȡ���ˮ���ᣨ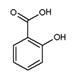 ����״��������õĶ����������������δ��Ӧ��ȫ��ˮ���ᣬ��Ҫ�����ᴿ�����˵�ϴ�Ӽ�Ϊ�� ��
����״��������õĶ����������������δ��Ӧ��ȫ��ˮ���ᣬ��Ҫ�����ᴿ�����˵�ϴ�Ӽ�Ϊ�� ��




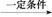 CH3CH2CH2CHO
CH3CH2CH2CHO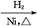 CH3CH2CH2CH2OH;CO���Ʊ�ԭ��:HCOOH
CH3CH2CH2CH2OH;CO���Ʊ�ԭ��:HCOOH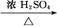 CO��+H2O,����Ƴ�ԭ�������Ʊ�װ��(��ͼ)��
CO��+H2O,����Ƴ�ԭ�������Ʊ�װ��(��ͼ)��