题目内容
【题目】根据如图所示的反应判断,下列说法中错误的是
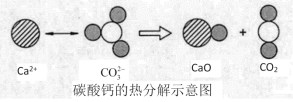
A.该反应的△H大于0
B.CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量
C.化学键断裂吸收能量,化学键形成放出能量
D.由该反应可推知:凡是需要加热才能发生的反应均为吸热反应
【答案】D
【解析】
碳酸钙为离子化合物,受热分解生成二氧化碳和氧化钙,是吸热反应,反应物总能量低于生成物,断键吸收的能量高于成键释放的能量,且与反应条件无关,以此解答该题。
A.根据分析,反应吸热,焓变大于零,故A正确;
B.反应吸热,生成物总能量高于反应物,CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量,故B正确;
C.断裂化学键需要吸收能量,形成化学键需要放出能量,故C正确;
D.反应是否放热与是否加热无关,如铝热反应放热,但需要在高温下进行,故D错误;
答案选D。

练习册系列答案
相关题目
【题目】下表是元素周期表的一部分,回答下列有关问题:
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
(1)①-中,属于长周期的元素是______![]() 填序号
填序号![]() 。
。
(2)①-![]() 填元素符号
填元素符号![]() ,在空气中燃烧的产物是______
,在空气中燃烧的产物是______![]() 写出电子式
写出电子式![]() 。
。
(3)①-中中,最不活泼的元素其原子结构示意图为______。
(4)③④⑤三种元素对应的简单阳离子中,半径最大的离子结构示意图为______。
(5)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是______![]() 写化学式
写化学式![]() 。
。
(6)若将④⑤的单质用导线相连插入稀硫酸溶液中形成原电池,则该原电池的负极反应式______。