题目内容
4.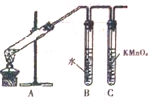 为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如图所示.回答:
为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如图所示.回答:(1)B装置的作用是吸收挥发出来的乙醇;
(2)若省去装置B、C装置中试剂应改为溴水,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
分析 溴乙烷与NaOH乙醇溶液发生消去反应生成乙烯,B中水可除去挥发的乙醇,C中乙烯被高锰酸钾氧化,或直接利用乙烯与溴水的加成反应来检验.
解答 解:(1)B装置的作用是吸收挥发出来的乙醇,故答案为:吸收挥发出来的乙醇;
(2)若省去装置B,C装置中试剂应改为溴水,发生的反应为CH2=CH2+Br2→CH2BrCH2Br,故答案为:溴水;CH2=CH2+Br2→CH2BrCH2Br.
点评 本题主要考查的是氯代烃的性质,为高频考点,侧重于学生的分析、实验能力的考查,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
相关题目
14.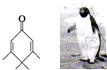 如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
 如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )
如图的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来取名为Penguinone.下列有关Penguinone的说法正确的是( )| A. | 若与Penguinone互为同分异构体的酚类且苯环上只有两个取代基的有机物有9种 | |
| B. | Penguinone分子中所有碳原子可能处于同一平面 | |
| C. | Penguinone分子中无酚羟基所以不能使酸性高锰酸钾溶液褪色 | |
| D. | Penguinone分子式为C10H14O |
12.碱性锌锰电池的总反应是:Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2,电解质是KOH.下列说法正确的是( )
| A. | MnO2发生了氧化反应 | |
| B. | MnOOH中Mn元素的化合价为+3 | |
| C. | 反应消耗 0.65g Zn,有0.01 mol电子发生转移 | |
| D. | 碱性锌锰电池是一种高效、环境友好的发电装置 |
9.欲除去小苏打溶液中的苏打杂质,加入的物质最宜选用( )
| A. | 二氧化碳 | B. | 盐酸 | C. | 碳酸氢钙 | D. | 氢氧化钙 |
16.在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中被氧化的元素( )
| A. | K | B. | H | C. | Mn | D. | Cl |
14.现有6瓶失去标签的液体,已知它们可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖中的一种.现通过如下实验来确定各试剂瓶中所装液体的名称:
(1)A的俗名为酒精,B中所含官能团的名称为羧基. D的结构简式为CH3COOCH2CH3.
(2)在D中加入NaOH溶液并加热的化学方程式为CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH.
(3)C的二氯代物有三种同分异构体;
(4)若将1mol乙醇(其中的羟基氧用18O标记)在浓硫酸存在下并加热与足量乙酸充分反应.则生成的乙酸乙酯的质量大于88g(填:大于,小于或等于)
(5)已知乙醛发生银镜反的方程式为:CH3CHO+2Ag(NH3)2OH$\stackrel{加热}{→}$CH3COONH4+H2O+2Ag↓+3NH3,试写出葡萄糖发生银镜反应的化学方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+H2O+3NH3.
| 实验步骤和方法 | 实验现象 |
| ①把6瓶液体分别依次标号A、B、C、D、E、F,然后闻气味 | 只有F没有气味 |
| ②各取少量于试管中,加水稀释 | 只有C、D、E不溶解而浮在水面上 |
| ③分别取少量6种液体于试管中,加新制Cu(OH)并加热 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
| ④各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
(2)在D中加入NaOH溶液并加热的化学方程式为CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH.
(3)C的二氯代物有三种同分异构体;
(4)若将1mol乙醇(其中的羟基氧用18O标记)在浓硫酸存在下并加热与足量乙酸充分反应.则生成的乙酸乙酯的质量大于88g(填:大于,小于或等于)
(5)已知乙醛发生银镜反的方程式为:CH3CHO+2Ag(NH3)2OH$\stackrel{加热}{→}$CH3COONH4+H2O+2Ag↓+3NH3,试写出葡萄糖发生银镜反应的化学方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH2OH(CHOH)4COONH4+2Ag↓+H2O+3NH3.

 .
.