题目内容
9.欲除去小苏打溶液中的苏打杂质,加入的物质最宜选用( )| A. | 二氧化碳 | B. | 盐酸 | C. | 碳酸氢钙 | D. | 氢氧化钙 |
分析 Na2CO3溶液可与二氧化碳反应生成NaHCO3,可用于除杂,以此解答.
解答 解:A.除去NaHCO3溶液中含有的Na2CO3溶质可在溶液中通入过量二氧化碳气体,Na2CO3溶液可与二氧化碳反应生成NaHCO3,故A正确;
B.碳酸钠和碳酸氢钠都能与盐酸反应,故B错误;
C.加入碳酸氢钙引入了新的杂质钙离子,故C错误;
D.氢氧化钙能与小苏打反应,将原物质除掉,故D错误.
故选A.
点评 本题考查物质的分离、提纯和除杂等问题,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A、容器中压强不变 B、混合气体中c(CO)不变
C、混合气体的密度不变 D、c(CO)=c(CO2)
E、化学平衡常数K不变 F、单位时间内生成CO的分子数与生成H2O的分子数相等
(4)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A、容器中压强不变 B、混合气体中c(CO)不变
C、混合气体的密度不变 D、c(CO)=c(CO2)
E、化学平衡常数K不变 F、单位时间内生成CO的分子数与生成H2O的分子数相等
(4)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
17.某化合物,其组成中没有C、H、O三种元素.这种化合物可能属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 有机物 |
14.对于反应:Zn+H2SO4=ZnSO4+H2↑,以下说法不正确的是( )
| A. | 该反应既是置换反应又是氧化还原反应 | |
| B. | Zn作还原剂,H2SO4作氧化剂 | |
| C. | Zn被氧化,H2SO4被还原 | |
| D. | 发生氧化反应的物质是H2SO4,发生还原反应的物质是Zn |
1.两气体A和B的摩尔质量之比为3:1,则它们在同温、同压、同体积时的分子个数比应为( )
| A. | 1:1 | B. | 1:3 | C. | 3:1 | D. | 9:1 |
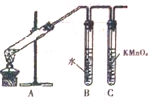 为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如图所示.回答:
为探究溴乙烷与NaOH乙醇溶液发生反应后生成的气体中是否含不饱和烃的装置如图所示.回答: